
| A. | 0.1mol/L | B. | 0.01mol/L | C. | 0.001mol/L | D. | 无法确定 |
科目:高中化学 来源: 题型:选择题
| A. | 向黄色溶液中加入淀粉,溶液变蓝色,则溶液中含有I2 | |
| B. | 向无色溶液中加入BaCl2溶液有白色沉淀出现,则溶液中含有SO42- | |
| C. | 用一束光照射氯化铁溶液和氢氧化铁胶体,都出现丁达尔现象 | |
| D. | 将AgNO3溶液滴入甲溶液中,若出现白色沉淀,则说明甲溶液中含有Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 “达菲”瑞士罗氏制药公司生产的一种治疗禽流感和甲型H1N1流感(猪流感)的特效药.达菲的主要有效成分莽草酸是从中国百姓常见的调味料八角茴香中提取出来的.莽草酸的结构式如图,下列说法正确的是( )
“达菲”瑞士罗氏制药公司生产的一种治疗禽流感和甲型H1N1流感(猪流感)的特效药.达菲的主要有效成分莽草酸是从中国百姓常见的调味料八角茴香中提取出来的.莽草酸的结构式如图,下列说法正确的是( )| A. | 它能使溴水褪色 | |
| B. | 遇FeCl3溶液呈紫色 | |
| C. | 它不能发生消去反应 | |
| D. | 1mol莽草酸跟足量的钠反应可以得到4molH2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 用高锰酸钾制取氧气 | |
| B. | 用乙酸和乙醇在浓硫酸作用下制取乙酸乙酯 | |
| C. | 碳酸氢钠受热分解 | |
| D. | 用氢氧化钙和氯化铵制取氨气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
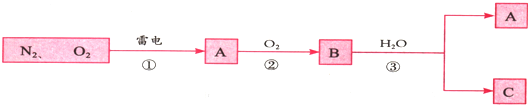
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业生产硫酸的过程中使用过量的氧气,以提高二氧化硫的转化率 | |
| B. | 使用催化剂能加快化学反应速率,提高产率 | |
| C. | 用氨的催化氧化法生产硝酸使用过量空气以提高氨气的利用率 | |
| D. | 实验室用排饱和食盐水法收集氯气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com