
某研究性学习小组从网上查到绿矾(FeSO4·7H2O)受热分解的方程式为:
2FeSO4·7H2O![]() Fe2O3+SO3↑SO3↑+14H2O↑,就设计了如下实验装置来验证绿矾受热分解是否发生上述反应。
Fe2O3+SO3↑SO3↑+14H2O↑,就设计了如下实验装置来验证绿矾受热分解是否发生上述反应。
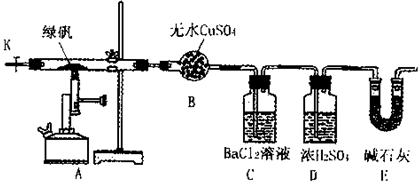
主要实验步骤如下:
①组装仪器并检查装置的气密性;
②称量绿矾样口及U型干燥管E的质量,将称量后的绿矾置于硬质玻璃管内;
③关闭活塞K,加强热使绿矾完全分解;
④打开活塞K,缓缓鼓入一定量的氮气;
⑤再次称量干燥管E的质量;
⑥重复④⑤的操作,直到干燥管E的质量基本不变为止;
⑦称量洗气瓶C中所得沉淀的质量。
试回答:
(1)洗气瓶D中浓H2SO4的作用为: ;
(2)步骤⑦从溶液中获取生成沉淀质量的具体操作为: ;
(3)实验小组的报告如下,请补充完整:
| 实验记录 | 分析或计算结果 | |
| 现象 | 硬质管内绿色变为红棕色; | 生成物有 |
| 干燥管B中晶体白色变蓝色。 | 生成物有H2O | |
| 数据 | 称取绿矾样品16.68g; | 反应的绿矾0.06mol |
| 干燥管E最后增重2.24g; | 生成SO2 mol | |
| C中生成白色沉淀的质量为4.66g; | 生成DO3 0.02mol |
(4)该实验所得到的数据与所样到的化学方程式中的定量关系不相符合,请分析可能的原因。
(5)为达到“验证绿矾受热分解是否发生上述反应”的目的,该实验的设计有多处不妥,请提出改进建议(两条即可)
(1)除去SO2中的H2O(或干燥) (2分)
(2)过滤、洗涤、干燥、称量 (2分)
(3)Fe2O3 (1分) 0.035 mol (1分)
(4)①高温下部分SO3分解为SO2和O2 ;
②干燥管E吸收了空气中的H2O和CO2气体;
③绿矾分解不完全;
④反应生成的气体未被完全吸收……
(只要答案合理均可,一条合理原因2分,共4分)
(5)增加检验SO2气体的装置,如将干燥管E换成装有品红试剂的洗气瓶等 ;
不必称量质量;
在装置最后再加上一个干燥管,防止空气中的水蒸气进入干燥管E中;
加尾气吸收装置,防止空气污染……
(其他合理答案均可,一条合理建议2分,共4分)
该实验具有一定的开放性,是试题发展的新趋势。验证生成的产物中有氧化铁、二氧化硫、三氧化硫、水,因大部分物质的验证需要经过水溶液,因此验证水放在第一位,无水硫酸铜与水反应得到五水硫酸铜,颜色有白色变为蓝色;三氧化硫通入到氯化钡溶液中将有白色沉淀生成,从而验证三氧化硫的存在;浓硫酸干燥二氧化硫,二氧化硫被碱石灰吸收,通过称重法验证二氧化硫的存在;氧化铁为红棕色,通过观察固体颜色的变化确定有氧化铁生成。


 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源: 题型:阅读理解


查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
 碘是人体必须的元素之一,海洋植物如海带、海藻中含有丰富的以碘离子形式存在的碘元素.海带中含有丰富的碘.为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
碘是人体必须的元素之一,海洋植物如海带、海藻中含有丰富的以碘离子形式存在的碘元素.海带中含有丰富的碘.为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
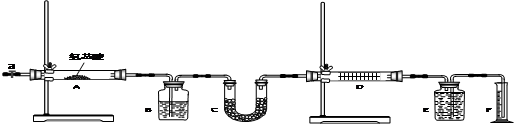
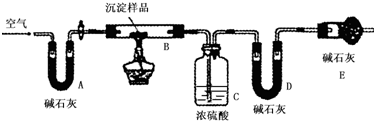
| B装置的质量(g) | C装置的质量(g) | D装置的质量(g) | |
| 实验前 | 15.4 | 262.1 | 223.8 |
| 试验后 | 6.1 | 264.8 | 230.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com