
| A. | 向FeI2溶液中滴加少量氯水,反应的离子方程式为:2Fe2++Cl2═2Fe3++2Cl- | |
| B. | 能使pH试纸显深红色的溶液中,Fe3+、Cl-、Ba2+、Br-,能够大量共存 | |
| C. | 向NaClO溶液中通入少量二氧化碳的离子方程式:2ClO-+CO2+H2O═2HClO+CO32- | |
| D. | 向溴水中加入足量氯化亚铁溶液能使溴水变成无色 |
分析 A.还原性Fe2+<I-,氯气先将碘离子氧化;
B.能使pH试纸显深红色的溶液是强酸性溶液;
C.碳酸酸性强于次氯酸,向NaClO溶液中通入少量二氧化碳能发生反应;
D.溴单质能将亚铁离子氧化为浅黄色的三价铁离子.
解答 解:A.还原性Fe2+<I-,向碘化亚铁中滴加少量氯水,氯气先将碘离子氧化,后氧化亚铁离子,故A错误;
B.能使pH试纸显深红色的溶液是强酸性溶液,强酸性溶液中Fe3+、Cl-、Ba2+、Br-能大量共存,故B正确;
C.碳酸酸性强于次氯酸,向NaClO溶液中通入少量二氧化碳的离子方程式:ClO-+CO2+H2O=HClO+HCO3-,故C错误;
D.氧化性:Br2>Fe3+,向溴水中加入足量氯化亚铁溶液溴单质能将亚铁离子氧化为浅黄色的三价铁离子,故D错误;
故选B.
点评 本题考查较为综合,涉及离子共存、离子方程式书写、氧化还原反应等知识,题目难度中等,明确常见元素及其 化合物性质为解答关键,试题培养了学生的灵活应用能力.


科目:高中化学 来源: 题型:选择题
| A. | CH3OH | B. | HOCH2CH(CH3)2 | C. | (CH3)3COH | D. | CH3CHOHCH2CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锂作为电池的负极,石墨作电池的正极 | |
| B. | 电池工作过程中,SOCl2被还原为Li2SO3 | |
| C. | 该电池内环境应该是无水环境,否则影响电池的寿命 | |
| D. | 电池工作时,锂提供的电子的物质的量与析出硫的物质的量之比是4:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| CH3COOH | HCN | H2CO3 |
| K=1.75×10-5 | K=4.9×10-10 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
| A. | 向NaCN溶液中通入少量CO2的离子方程式:CN-+H2O+CO2═HCN+HCO3- | |
| B. | 25℃时,反应CH3COOH+CN-?HCN+CH3COO-的化学平衡常数为3.57×104 | |
| C. | 中和等体积、等物质的量浓度的CH3COOH和HCN溶液,消耗NaOH的量前者小于后者 | |
| D. | 等物质的量浓度的CH3COONa和NaCN混合溶液中:c(CH3COO-)>c(CN-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在密闭容器中充入4molNH3与足量氧气充分反应,达到平衡时放出热量为3623KJ | |
| B. | 平衡时v正(O2)=$\frac{4}{5}$ v逆(NO) | |
| C. | 平衡后降低压强,混合气体平均摩尔质量减小 | |
| D. | 平衡后升高温度,混合气体中NO含量增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 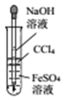 所示装置制取并观察Fe(OH)2 | |
| B. |  所示装置制取金属锰 | |
| C. | 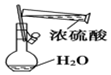 所示装置配制100 mL 0.1 mol•L-1 硫酸溶液 | |
| D. |  所示装置比较N、C、Si的非金属性强弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 能源问题是人类社会面临的重大课题.甲醇是未来重要的绿色能源之一.
能源问题是人类社会面临的重大课题.甲醇是未来重要的绿色能源之一.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 反应①②中都存在:△S>0 | B. | 反应②高温时,可自发进行 | ||
| C. | 在通常情况下,①②都能自发进行 | D. | 反应①一定不能自发进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应方程式中,x=1 | B. | 2min时,A的转化率为50% | ||
| C. | 2min时,A的物质的量为0.75mol | D. | 反应速率v(B)=0.25 mol•L-1•min-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com