
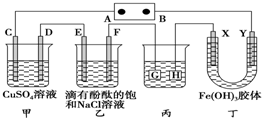
分析 (1)将直流电源接通后,F极附近呈红色,可知道氢离子在该电极放电,所以F即是阴极,并得到其他各个电极的名称,硫酸铜中铜离子减少导致溶液颜色的变化,胶体的胶粒带电,即电泳实验证明的结论;
(2)电镀时,镀层Ag为阳极、镀件Cu为阴极,电解质溶液为AgNO3溶液,根据转移电子相等计算析出Ag的质量;
(3)根据转移电子相等进行计算其物质的量之比;
(4)若将C换为Ag,则阳极上Ag失电子、阴极上Cu离子放电;
(5)Ag+和Cl-反应生成AgCl沉淀,电解时溶液中不存在Ag+,阴离子放电顺序为Cl->OH-,若在一极析出0.3molCu,阴极得到电子为0.3mol×2=0.6mol,结合两极转移电子数目相等以及电极方程式计算.
解答 解:将直流电源接通后,F极附近呈红色,说明F极显碱性,是氢离子在该电极放电,所以F即是阴极,可得出D、F、H、Y均为阴极,C、E、G、X均为阳极,A是电源的正极,B是负极;
(1)B电极是电源的负极,在A池中,电解硫酸铜的过程中,铜离子逐渐减少,导致溶液颜色变浅,Y极是阴极,该电极颜色逐渐变深,说明氢氧化铁胶体向该电极移动,异性电荷相互吸引,所以氢氧化铁胶体粒子带正电荷,
故答案为:负极;逐渐变浅;氢氧化铁胶体粒子带正电荷;
(2)电镀装置中,镀层金属必须做阳极,镀件做阴极,含有银离子的溶液为电解质溶液,则电镀液为AgNO3溶液,H应该是镀件,当乙中溶液的pH是13时(此时乙溶液体积为500mL)时,根据电极反应2H++2e-═H2↑,则放电的氢离子的物质的量为:0.1mol/l×0.5L=0.05mol,当转移0.05mol电子时,丙中镀件上析出银的质量=108g/mol×0.05mol=5.4g,电解硫酸铜的过程中氢氧根减少,所以氢离子浓度增大,所以酸性增强,甲中溶液的pH 变小,
故答案为:镀件;AgNO3;变小;5.4g;
(3)C、D、E、F发生的反应分别为:4OH--4e-=2H2O+O2↑、Cu2++2e-=Cu、2Cl--2e-=Cl2↑、2H++2e-=H2↑,串联电路中转移电子相等,假设都转移4mol电子时,O2、Cu、Cl2、H2的物质的量分别是1mol、2mol、2mol、2mol,所以生成单质的物质的量之比为1:2:2:2,
故答案为:1:2:2:2;
(4)若将C换为Fe,则阳极上Fe失电子、阴极上Cu离子放电,电池反应式为Fe+Cu2+$\frac{\underline{\;电解\;}}{\;}$Cu+Fe2+,故答案为:Fe+Cu2+$\frac{\underline{\;电解\;}}{\;}$Cu+Fe2+.
(5)Ag+和Cl-反应生成AgCl沉淀,电解时溶液中不存在Ag+,
反应后溶液中存在0.4molCu2+、0.4molCl-,
若在一极析出0.3molCu,阴极得到电子为0.3mol×2=0.6mol,
阳极首先发生:2Cl--2e-=Cl2↑,然后发生4OH--4e-=O2+2H2O,
则0.4molCl-生成0.2molCl2,失去0.4mol电子,在反应中4OH--4e-=O2+2H2O,转移0.2mol电子,生成0.05molO2,
则气体的体积为(0.2mol+0.05mol)×22.4L/mol=5.6L;
故答案为:5.6.
点评 本题考查电解原理的应用,正确判断阴阳极及正负极是解本题关键,知道各个电极上发生的反应,会正确书写电极反应式,题目难度中等,侧重于考查学生对基础知识的综合应用能力和计算能力.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质子数c>d | B. | 离子的还原性Y2->Z- | ||
| C. | 离子半径aW3+>cY2- | D. | 原子半径X<W |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | Al | B | Be | C | Cl | F | Li |
| x的数值 | 1.5 | 2.0 | 1.5 | 2.5 | 2.8 | 4.0 | 1.0 |
| 元素 | Mg | Na | O | P | S | Si | |
| x的数值 | 1.2 | 0.9 | 3.5 | 2.1 | 2.5 | 1.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1molC3H6Cl2中化学键总数为NA | |
| B. | 14g乙烯和丙烯混合气体中含原子数为3NA | |
| C. | 标准状况下,1L苯完全燃烧生成的气态产物的分子数为$\frac{6}{22.4}$NA | |
| D. | 0.1NA乙醇分子完全燃烧所消耗的氧气为0.3mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子化合物中一定含有离子键 | |
| B. | 单质分子中均不存在化学键 | |
| C. | 含活泼金属元素的化合物一定不是共价化合 | |
| D. | 含有共价键的化合物一定是共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
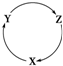 下表各组物质中,不满足下图物质一步转化关系的选项是( )
下表各组物质中,不满足下图物质一步转化关系的选项是( )| 选项 | X | Y | Z |
| A | NO2 | HNO3 | NO |
| B | Cu | CuSO4 | Cu(OH)2 |
| C | Al2O3 | NaAlO2 | Al(OH)3 |
| D | SiO2 | Na2SiO3 | H2SiO3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ④ | ⑤ | ⑥ | ⑦ | ||||
| 3 | ② | ③ | ⑧ | ⑩ | ||||
| 4 | ① | ⑨ |
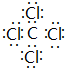 ,该分子含有极性(填“极性”或“非极性”)键;⑤元素形成的单质的结构式为N≡N⑧元素形成简单离子的结构示意图为
,该分子含有极性(填“极性”或“非极性”)键;⑤元素形成的单质的结构式为N≡N⑧元素形成简单离子的结构示意图为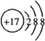 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com