
| A. | Na+,Fe3+,NO3-,Cl- | B. | K+,Na+,Cl-,SO42- | ||
| C. | K+,CO32-,Na+,Cl- | D. | Mg2+,Cl-,K+,SO42- |
分析 无色溶液中不含有色离子,与铝反应生成氢气说明溶液呈强酸性或强碱性,酸为非强氧化性酸,且离子之间不能生成气体、沉淀、弱电解质、双水解等,据此分析解答.
解答 解:A.Fe3+呈黄色,不符合无色条件,故A选;
B.这几种离子都呈无色,且离子之间不反应,且和氢离子或氢氧根离子都不反应,所以可以大量共存,故B不选;
C.这几种离子都呈无色,碱性条件下,能大量共存,碱性条件下与铝反应生成氢气,所以可以大量共存,故C不选;
D.这几种离子都呈无色,酸性条件下,离子之间不反应,且酸性条件下铝和酸反应生成氢气,故D不选;
故选A.
点评 本题考查离子共存,为高频考点,侧重考查复分解反应和氧化还原反应,明确离子的性质是解本题关键,注意硝酸和铝反应生成氮氧化物而不是氢气,为易错点.


 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案科目:高中化学 来源: 题型:选择题
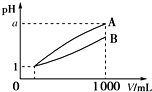 pH=1的两种酸溶液A、B各1mL,分别加水稀释到1 000mL,其pH与溶液体积(V)的关系如图所示,下列说法不正确的是( )
pH=1的两种酸溶液A、B各1mL,分别加水稀释到1 000mL,其pH与溶液体积(V)的关系如图所示,下列说法不正确的是( )| A. | 若a=4,则A是强酸,B是弱酸 | |
| B. | 稀释后,A酸溶液的酸性比B酸溶液强 | |
| C. | A、B两种酸溶液的物质的量浓度一定不相等 | |
| D. | 若1<a<4,则A、B都是弱酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | MgCO3、MgO、Mg3N2 | B. | Mg(OH)2、MgO、MgCO3 | C. | MgO、Mg3N2、C | D. | Mg3N2、C、MgCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AgCl 和Ag2CrO4 的溶解度相等 | |
| B. | 由Ksp的相对大小可以直接判断出AgCl的溶解度大于 Ag2CrO4 | |
| C. | 两者类型不同,不能由Ksp的大小直接判断溶解能力的大小 | |
| D. | 都是难溶盐,溶解度无意义 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图是某空间站能量转化系统的局部示意图,其中燃料电池采用KOH为电解液,下列有关说法中不正确的是( )
如图是某空间站能量转化系统的局部示意图,其中燃料电池采用KOH为电解液,下列有关说法中不正确的是( )| A. | 燃料电池系统产生的能量实际上来自于水 | |
| B. | 该能量转化系统中的水也是可能循环的 | |
| C. | 水电解系统中的阳极反应:4OH--4e-=2H2O+O2↑ | |
| D. | 燃料电池放电时的负极反应:H2-2e-+2OH-=2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.22g | B. | 0.55g | C. | 0.44g | D. | 0.66g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.0×10-7 mol•L-1 | B. | 0.1×10-7 mol•L-1 | ||
| C. | 1.0×10-14/2.0×10-7 mol•L-1 | D. | 无法确定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com