
在1LK2SO4和CuSO4的混合溶液中,c(SO42﹣)=2.0mol•L﹣1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4L(标况)气体,则原溶液中K+的物质的量浓度为( )
|
| A. | 2.0mol•L﹣1 | B. | 1.5mol•L﹣1 | C. | 1.0mol•L﹣1 | D. | 0.5mol•L﹣1 |
考点:
电解原理.
专题:
电化学专题.
分析:
根据电解池中离子的放电顺序和两极上发生的变化来书写电极反应方程式,并且两个电极上转移的电子数目是相等的,溶液中遵循电荷守恒.
解答:
解:电解1LK2SO4和CuSO4的混合溶液,阳极发生的反应为:4OH﹣→2H2O+O2↑+4e﹣,阴极上发生的电极反应为:Cu2++2e﹣→Cu,2H++2e﹣→H2↑,两极均收集到22.4L(标况)气体,即均生成1mol的气体,阳极生成1mol氧气说明转移了4mol电子,而阴极上生成的1molH2只得到了2mol电子,所以剩余2mol电子由铜离子获得,且溶液中有1mol铜离子,再根据溶液为电中性,遵循电荷守恒可得钾离子物质的量为2×2﹣1×2=2mol,所以浓度为2mol/L.
故选A.
点评:
本题考查学生电解池的工作原理以及溶液中的电荷守恒思想,难度不大,可以根据所学知识来回答.


科目:高中化学 来源: 题型:
黄曲霉素是污染粮食的真菌霉素,其结构如图,人类的特殊基因在黄曲霉素的作用下会发生突变,有转变成肝癌的可能性.下列的说法正确的是( )

|
| A. | 黄曲霉素能发生取代反应和消去反应 |
|
| B. | 1mol黄曲霉素能与6mol氢气发生加成反应 |
|
| C. | 1mol黄曲霉素能与含1mol NaOH的水溶液完全反应 |
|
| D. | 黄曲霉素能与溴水反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
|
| A. | ⅠA族元素单质的熔点从上往下逐渐降低 |
|
| B. | 分子晶体中一定存在共价键 |
|
| C. | ⅥA族元素的氢化物中,稳定性最好的其沸点也最高 |
|
| D. | 同周期非金属氧化物对应的水化物的酸性从左往右依次增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知铍(Be)的原子序数为4.下列对铍及其化合物的叙述中,正确的是( )
|
| A. | 铍的原子半径小于硼的原子半径 |
|
| B. | 氧化铍分子中铍原子的最外层电子数是8 |
|
| C. | 氢氧化铍的碱性比氢氧化钙的弱 |
|
| D. | 单质铍跟冷水反应产生氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
将质量相等的铁片和铜片用导线相连浸入500mL硫酸铜溶液中构成如图1的装置:(以下均假设反应过程中溶液体积不变).
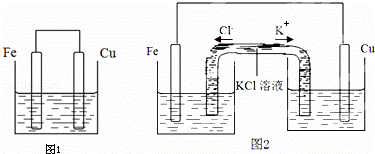
(1)铁片上的电极反应式为 .
(2)铜片周围溶液会出现 的现象.
(3)若2min后测得铁片和铜片之间的质量差为1.2g,计算:
①导线中流过的电子的物质的量为 mol;
②该段时间内用硫酸铜表示的平均反应速率为 mol•L﹣1•min﹣1
(4)若一段时间后测得铁片减少了2.4g,同时铜片增加了3.2g,计算这段时间内该装置消耗的化学能转化为电能的百分比为 .
(5)若将该装置改为如图2所示的装置也能达到和原装置相同的作用.其中KCl溶液起沟通两边溶液形成闭合回路的作用,同时又能阻止反应物直接接触.则硫酸铜溶液应该注入 (填“左侧”、“右侧”或“两侧”)烧杯中.
查看答案和解析>>
科目:高中化学 来源: 题型:
向含有NaBr、KI的溶液中通入过量的Cl2,然后将溶液蒸干,并灼烧固体,最后得到的物质是( )
|
| A. | KCl | B. | NaCl和KCl | C. | NaCl和KBr | D. | NaCl、KCl和I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中只含有Na+、Al3+、Cl﹣、SO42﹣ 四种离子,已知前三种离子的个数比为3:2:1,则溶液中Al3+和 SO42﹣的离子个数比为( )
|
| A. | 1:2 | B. | 1:4 | C. | 3:4 | D. | 3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)⇌CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为 ;
(2)反应是 反应.(选填“吸热”、放热).
(3)能判断该反应是否达到化学平衡状态的依据是 .
a.容器中压强不变 b.混合气体中c(CO)不变
c.v正(H2)=v逆(H2O) d.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)•c(CH2)=c(CO)•c(H2O),试判断此时的温度为 ℃
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com