
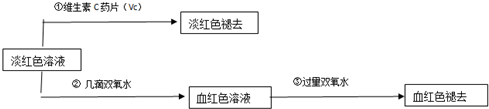
分析 (1)根据亚铁离子的化学性质及甲、乙同学的操作是否严密进行分析;
(2)根据三价铁离子具有氧化性及淡黄色褪去判断维生素具有的性质;
(3)加入氯水,亚铁离子被氧化成了三价铁离子;硫氰化钾与铁离子生成硫氰化铁;
(4)学生丙将乙所得的淡红色溶液分成两份,其中一份加入几滴双氧水,溶液变为血红色,说明铁离子浓度增大结合硫氰酸根离子形成血红色溶液,加入过量过氧化氢溶液血红色褪去,可能是过量的双氧水与Fe3+结合生成了某种稳定的新物质;另一种则是过量的双氧水将SCN-氧化了,可以向反应后的溶液中重新加入硫氰化钾溶液,根据现象判断两种假设的合理性,另一份加入维生素C淡红色退去说明铁离子被维生素C还原为亚铁离子,
(5)根据题中信息找出本次实验尚未完成的任务.
解答 解:(1)由于亚铁离子容易被空气中的氧气氧化,乙同学动作敏捷,且在振荡前用橡皮塞塞紧试管口,而甲同学充分振荡后,慢慢加入稀硫酸,所以乙同学比较合理,
故答案为:乙; 亚铁盐在空气中易被氧气氧化;
(2)由于三价铁离子具有氧化性,加入维生素后淡红色褪去,铁离子被维生素还原成了亚铁离子,
故答案为:还原;
(3)②中现象对应的反应方是氯气和亚铁离子的反应及硫氰化钾与铁离子反应生成血红色的硫氰化铁,反应的离子方程式是:2Fe2++Cl2=2 Fe3++2Cl-,Fe3++3SCN-═Fe(SCN)3,
故答案为:2Fe2++Cl2=2Fe3++2Cl-、Fe3++3SCN-═Fe(SCN)3;
(4)若是氯水将SCN-氧化了,可以重新加入硫氰化钾溶液,观察现象,如果变成血红色,第二种假设合理;如果不变色,说明第一种假设合理,
故答案为:再加过量KSCN溶液,如果变血红色,则第二种合理;如果不变色,则第一种合理;
(5)根据“某研究性学习小组为探究其主要成分,进行了如下实验”,本次实验尚未完成的任务是:未能测出“速力菲”成分,
故答案为:未能测其成分.
点评 本题考查了探究“速力菲”主要成分,充分考查了学生的分析、理解能力及对所学知识的掌握情况,本题难度中等.


 活力课时同步练习册系列答案
活力课时同步练习册系列答案科目:高中化学 来源: 题型:选择题
| A. | 取少许某溶液,滴加数滴KSCN溶液,无明显现象;再另取少许原溶液,先滴少量新制氯水,再滴加数滴KSCN溶液,溶液变血红色,则原溶液中一定含Fe2+ | |
| B. | 焰色反应时,用稀硫酸洗净铂丝,并在火焰上灼烧至无色,然后蘸取溶液 | |
| C. | 在淀粉溶液中加入稀硫酸并加热片刻后,再加入适量银氨溶液,水浴加热后没有银镜生成,说明淀粉没有水解 | |
| D. | 测定某溶液的pH,常用干燥洁净的玻璃棒蘸取该溶液滴在润湿的pH试纸上 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 16 g O2所含的原子数目为NA | |
| B. | 0.5 mol H2O2含有的原子数目为1.5NA | |
| C. | 1 mol H2O含有的H2O分子数目为NA | |
| D. | 0.5NA个氯气分子的物质的量是0.5 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NF3中只含有极性共价键 | |
| B. | NF3既是氧化产物,又是还原产物 | |
| C. | NH4F中既含有离子键又含有共价键 | |
| D. | 上述反应中,反应物和生成物均属于共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲苯分子中共平面的原子最多是12个 | |
| B. | 对二甲苯分子中有4个碳原子在一条直线上 | |
| C. | 1-丁烯分子中的4个碳原子一定不在同一平面内 | |
| D. | 2-丁烯分子中的4个碳原子一定不在同一平面内 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加热 | B. | 不用稀硫酸,改用98%浓硫酸 | ||
| C. | 加入硫酸铜 | D. | 不用铁片,改用铁粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com