
【题目】室温下,将0.1mol/L的一元酸HA溶液逐滴滴加到10mL0.1mol/LNaOH溶液中,pH的变化曲线如图所示。下列说法错误的是

A. a点所示溶液中c(Na+)>c(A-)>c(OH-)>c(HA)
B. a、b两点所示溶液中水的电离程度a点大于b点
C. pH=7时,c(Na+)=c(A-)+c(HA)
D. 一元酸HA为弱酸
【答案】C
【解析】A. a点时加入10mL的一元酸HA,酸碱恰好中和得到NaA溶液,溶液的pH=8.7,说明NaA为强碱弱酸盐,A-发生水解反应A-+H2O![]() HA+ OH-且水解是微弱的,则c(Na+)>c(A-)>c(OH-),因水也电离产生OH-,则c(OH-)>c(HA),所以微粒浓度大小顺序为:c(Na+)>c(A-)>c(OH-)>c(HA),故A正确;B. a点时溶液中只有NaA,A-发生水解促进水的电离,b点溶液中酸过量,酸抑制水的电离,所以a、b两点所示溶液中水的电离程度a点大于b点,故B正确;C. pH=7时,c(H+)=c(OH-),由电荷守恒可知,c(Na+)+ c(H+)=c(A-)+c(OH-),则c(Na+)=c(A-),故C错误;D. 根据A项分析可知,HA为一元弱酸,故D正确;答案选C。
HA+ OH-且水解是微弱的,则c(Na+)>c(A-)>c(OH-),因水也电离产生OH-,则c(OH-)>c(HA),所以微粒浓度大小顺序为:c(Na+)>c(A-)>c(OH-)>c(HA),故A正确;B. a点时溶液中只有NaA,A-发生水解促进水的电离,b点溶液中酸过量,酸抑制水的电离,所以a、b两点所示溶液中水的电离程度a点大于b点,故B正确;C. pH=7时,c(H+)=c(OH-),由电荷守恒可知,c(Na+)+ c(H+)=c(A-)+c(OH-),则c(Na+)=c(A-),故C错误;D. 根据A项分析可知,HA为一元弱酸,故D正确;答案选C。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】肼(N2H4,无色液体)是一种用途广泛的化工原料。实验室中先制备次氯酸钠,再用次氯酸钠溶液和氨反应制备肼并验证肼的性质。实验装置如图所示。
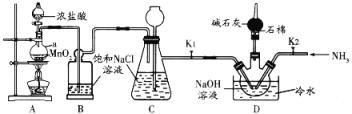
已知:Cl2(g)+2NaOH(aq)=NaC1O(aq)+NaC1(aq)+H2O(g) △H<0。当温度超过40℃时,Cl2与NaOH溶液反应生成NaClO3。回答下列问题:
(1)仪器a的名称是________________,装置B的作用是____________________________。
(2)为控制D装置中的反应温度,除用冷水浴外,还需采取的实验操作是________________。
(3)当三颈烧瓶中出现黄绿色气体时立即关闭分液漏斗活塞、移去酒精灯、关闭K1。此时装置C的作用是________________________________。
(4)将D装置水槽中的冷水换为热水,把三颈烧瓶中黄绿色气体赶走后,打开K2,通入NH3,使其与NaC1O溶液反应制取肼。理论上通入三颈烧瓶的Cl2和NH3的最佳物质的量之比为______________。
(5)请从提供的下列试剂中选择合适试剂,设计合理的实验方案验证肼的还原性____________(说明操作、现象和结论)。
①淀粉-KI溶液 ②稀硫酸(酚酞) ③NaHCO3 ④AgC1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将32.64 g Cu与200 mL一定浓度的HNO3反应,Cu完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2 L。
(1)求生成NO的物质的量;____________________
(2)求生成NO2的体积。____________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH4和H2O(g)可发生催化重整反应:CH4(g)+H2O(g)![]() CO(g)+3H2(g)。
CO(g)+3H2(g)。
(1)每消耗8g CH4转移的电子的数目为________________。
(2)已知:①2CO(g)+O2(g)=2CO2(g) △H1=akJ·mol-1
②CO(g)+H2O(g)=CO2(g)+H2(g)△H2=bkJ·mol-1
③CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H3=ckJ·mol-1
④CH4(g)+H2O(g)![]() CO(g)+3H2(g) △H4
CO(g)+3H2(g) △H4
由此计算△H4=_____________kJ·mol-1。
(3)T℃时,向1L恒容密闭容器中投入1molCH4和1molH2O(g),发生反应:CH4(g)+H2O(g)![]() CO(g)+3H2(g),经过tmin,反应达到平衡。已知平衡时,c(CH4)=0.5mol·L-1。
CO(g)+3H2(g),经过tmin,反应达到平衡。已知平衡时,c(CH4)=0.5mol·L-1。
①0~tmin内,该反应的平均反应速率v(H2)=___________。
②T℃时,该反应的甲烷的转化率是_________。
③下列表述能作为反应达到化学平衡状态的标志是_____________。
a.反应速率v(CH4):v(H2) =1:3 b.各组分的物质的量浓度不再改变
c.混合气体的平均相对分子质量不再改变 d.混合气体的密度不变
e.单位时间内生成n molH2O的同时,生成3n mol H2 f.单位时间内4mol C—H键断裂的同时2mol O—H键也断裂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,可逆反应A(g)+3B(g)![]() 2C(g)达到平衡的标志是( )
2C(g)达到平衡的标志是( )
A. 单位时间内消耗1molA的同时生成2molC
B. 单位时间内消耗nmolA的同时生成2nmolB
C. A、B、C的物质的量之比为1:2:3
D. A、B、C的浓度不再发生变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量纯净的氨基甲酸铵置于密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:H2NCOONH4(s)![]() 2NH3(g)+CO2(g)。能判断该反应已经达到化学平衡的是( )
2NH3(g)+CO2(g)。能判断该反应已经达到化学平衡的是( )
①v(NH3)正=2v(CO2)逆 ②密闭容器中总压强不变 ③密闭容器中混合气体的密度不变 ④密闭容器中混合气体的平均相对分子质量不变 ⑤密闭容器混合气体的总物质的量不变⑥密闭容器中CO2的体积分数不变 ⑦ 混合气体总质量
A. ①②③⑤⑦ B. ①②⑤⑦ C. ①⑤⑥ D. 全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式表示正确的是 ( )
A. 往FeI2溶液中通入过量氯气:Cl2+2Fe2+===2Cl-+2Fe3+
B. 将明矾溶于水中生成胶体:Al3++3H2O![]() Al(OH)3(胶体)+3H+
Al(OH)3(胶体)+3H+
C. 大理石溶于醋酸中:CaCO3+2H+===Ca2++H2O+CO2↑
D. 铜与稀硝酸反应:3Cu+4H++2NO3-===3Cu2++2NO↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知-NH2表现碱性,-NO2和![]() 表现中性,-COOH表现酸性。化学式为C7H7NO2的有机物,其分子结构中有1个苯环、2个取代基,试按照下列写出4种同分异构体(只写邻位即可)。
表现中性,-COOH表现酸性。化学式为C7H7NO2的有机物,其分子结构中有1个苯环、2个取代基,试按照下列写出4种同分异构体(只写邻位即可)。
(1)该有机物只有酸性______________________。
(2)该有机物只有碱性______________________。
(3)该有机物既有酸性又有碱性______________。
(4)该有机物既无酸性又无碱性______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com