
分析 (1)若A是非金属单质,X是强氧化性单质,C与水反应生成强酸,则C是酸性氧化物,且A含有多种正化合价,则A为S或N2;
(2)若A是一种铁矿石,反应①和②都是工业制硫酸生产中的重要反应,C与水反应生成强酸D,则X是氧气,B是二氧化硫,C是三氧化硫,D是硫酸.
解答 解:(1)若A是非金属单质,X是强氧化性单质,C与水反应生成酸,则C是酸性氧化物,且A含有多种正化合价,则A为S或C或N2,X是强氧化剂氧气,
故答案为:S或N2;
(2)若A是一种铁矿石,反应①和②都是工业制硫酸生产中的重要反应,C与水反应生成强酸D,则X是氧气,B是二氧化硫,C是三氧化硫,D是硫酸,铜和浓硫酸反应生成硫酸铜、二氧化硫和水,反应方程式为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,
故答案为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O.
点评 本题考查无机物的推断,本题侧重于元素化合物知识,明确物质的性质是解本题关键,难度中等.


 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 因为s轨道的形式是球形的,所以处于s轨道上的电子做的是圆周运动 | |
| B. | 电子在3px、3py、3ps三个轨道上运动时,能量不同 | |
| C. | 电子云是用来形象的描述电子运动状态的 | |
| D. | H、F、Cl、O的电负性逐渐增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
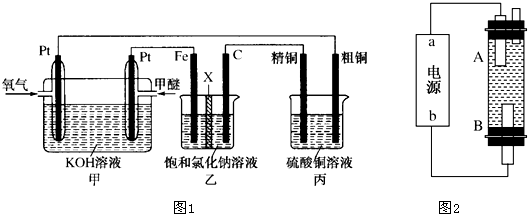
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 36g H2O中含有氧原子数为2NA | |
| B. | 标准状况下,11.2L苯所含分子数为0.5NA | |
| C. | 1L 1 mol•L-1硫酸钠溶液中,所含钠离子数为NA | |
| D. | 1mol H2在O2中完全燃烧转移的电子数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
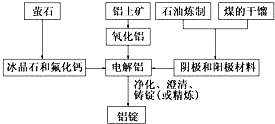 如图是传统的工业生产金属铝的基本流程图.结合铝生产的流程图回答下列问题:
如图是传统的工业生产金属铝的基本流程图.结合铝生产的流程图回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com