
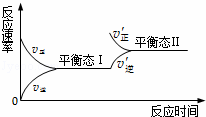
如图是恒温下某化学反应的反应速率随反应时间变化的示意图.下列叙述与示意图不相符合的是( )
|
| A. | 反应达平衡时,正反应速率和逆反应速率相等 |
|
| B. | 该反应达到平衡态Ⅰ后,增大反应物浓度,平衡发生移动,达到平衡态Ⅱ |
|
| C. | 该反应达到平衡态后,减小反应物浓度,平衡发生移动,达到平衡态Ⅱ |
|
| D. | 同一种反应物在平衡态Ⅰ和平衡Ⅱ时浓度不相等 |
考点:
化学反应速率与化学平衡图象的综合应用.
专题:
压轴题;化学平衡专题.
分析:
由图可知,该反应从正反应一端开始,正逆反应速率相等时为状态Ⅰ,然后,该反应向正反应方向移动,正反应速率大于逆反应速率,且改变条件的一瞬间逆反应速率不变,以此来解答.
解答:
解:A.由平衡的特征可知,反应达平衡时,正反应速率和逆反应速率相等,故A正确;
B.该反应达到平衡态Ⅰ后,增大反应物浓度,一瞬间正反应速率增大,逆反应速率不变,平衡正向移动,达到平衡态Ⅱ,故B正确;
C.该反应达到平衡态后,减小反应物浓度,平衡应逆向移动,逆反应速率大于正反应速率,与图象矛盾,故C错误;
D.该反应达到平衡态Ⅰ后,改变条件使反应继续正向移动达到平衡态Ⅱ,所以同一种反应物在平衡态Ⅰ和平衡Ⅱ时浓度不相等,故D正确;
故选C.
点评:
本题考查化学反应速率与化学平衡的图象,明确图象中状态Ⅰ到平衡态Ⅱ正反应速率大于逆反应速率及瞬间逆反应速率不变时解答本题的关键,题目难度中等.


科目:高中化学 来源: 题型:
已知反应2SO2(g)+O2(g)⇌2SO3(g)△H<0,向某体积恒定的密闭容器中按体积比2:1充入SO2和O2,在一定条件下发生反应.下图是某物理量(Y)随时间(t)变化的示意图(图中T表示温度),Y可以是( )

|
| A. | SO2的转化率 | B. | 混合气体的密度 |
|
| C. | 密闭容器内的压强 | D. | O2的体积分数 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列几种氢键:①O—H…O、②N—H…N、③F—H…F、④O—H…N,按氢键从强到弱的顺序正确的是
| A.③>①>④>② | B.①>②>③>④ |
| C.③>②>①>④ | D.①>④>③>② |
查看答案和解析>>
科目:高中化学 来源: 题型:
室温时,下列混合溶液的pH一定小于7的是( )
|
| A. | pH=3的盐酸和pH=11的氨水等体积混合 |
|
| B. | pH=3的盐酸和pH=11的氢氧化钡溶液等体积混合 |
|
| C. | pH=3的醋酸和pH=11的氢氧化钡溶液等体积混合 |
|
| D. | pH=3的硫酸和pH=11的氨水等体积混合 |
查看答案和解析>>
科目:高中化学 来源: 题型:
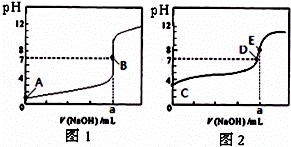
常温下,用0.1000mol/L NaOH溶液分别滴定20.00mL 0.1000mol/L 盐酸和20.00mL 0.1000mol/L 醋酸溶液,得到2条滴定曲线,如图所示.若以HA表示酸,下列说法正确的是( )
|
| A. | 滴定盐酸的曲线是图2 |
|
| B. | 达到B、D状态时,两溶液中离子浓度均为 c(Na+)=c(A﹣) |
|
| C. | 达到B、E状态时,反应消耗的n(CH3COOH)>n(HCl) |
|
| D. | 当0 mL<V(NaOH)<20.00 mL时,对应混合溶液中各离子浓度由大到小的顺序均为 c(A﹣)>c(Na+)>c(H+)>c(OH﹣) |
查看答案和解析>>
科目:高中化学 来源: 题型:
恒温、恒压下,在一个可变容积的容器中发生如下反应:A(g)+B(g)⇌C(g)
(1)若开始时放入1mol A+1mol B,到达平衡后,生成a mol C,这时A的物质的量为 mol.
(2)若开始时放入3mol A和3mol B,到达平衡后,生成C的物质的量为 mol.
(3)若开始时放入x mol A,2mol B和1mol C,到达平衡后,A和C的物质的量分别为y mol和3a mol,则x= mol,y= mol.平衡时,B的物质的量 (选填一个编号).
(甲)大于2mol (乙)等于2mol (丙)小于2mol (丁)可能大于、等于或小于2mol
(4)若在(3)的平衡混合物中再加入3mol C,待再次达到平衡后,C的物质的量分数是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
萤火虫发光前后物质的变化如下:

下列关于荧光素和氧化荧光素的叙述不正确的是( )
|
| A. | 二者的分子组成相差一个CHO |
|
| B. | 二者的分子组成相差一个CH2O |
|
| C. | 二者都能与浓溴水反应且每摩尔消耗Br2的量相同 |
|
| D. | 都能使酸性KMnO4溶液褪色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com