



科目:高中化学 来源: 题型:
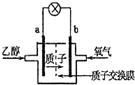 乙醇燃料电池中采用磺酸类质子溶剂,在200℃左右时供电,电池总反应为:C2H5OH+3O2?2CO2+3H2O,电池示意如图.下列说法中,正确的是( )
乙醇燃料电池中采用磺酸类质子溶剂,在200℃左右时供电,电池总反应为:C2H5OH+3O2?2CO2+3H2O,电池示意如图.下列说法中,正确的是( )| A、电池工作时,质子向电池的负极迁移 | B、1mol乙醇被氧化时转移电子数为6mol | C、a极上发生的电极反应是:C2H5OH+3H2O+12e-?2CO2+12H+ | D、用此电池给铅蓄电池充电,消耗4.8g O2时生成0.6mol H2SO4 |
查看答案和解析>>
科目:高中化学 来源:三点一测丛书 高中化学(选修)化学反应原理 江苏版课标本 江苏版课标本 题型:038
铅蓄电池具有电压高,放电容量大,经济上较便宜等特点,广泛用于汽车、拖拉机、轮船做启动与照明电源.已知:铅蓄电池充电完毕后,电池中硫酸的密度为ρ1,放电完毕后,溶液的密度变为ρ2.又铅蓄电池放电和充电时的反应:Pb+PbO2+2H2SO4![]() 2PbSO4+2H2O如图所示的装置,表示铅蓄电池工作示意简图试回答:
2PbSO4+2H2O如图所示的装置,表示铅蓄电池工作示意简图试回答:

(1)写出铅蓄电池(装置甲)工作时电极反应方程式:________.
(2)写出装置甲工作一段时间后,装置乙中A、B两端观察到的现象.写出有关反应的电极方程式________.
(3)已知充、放电完毕后,溶液的密度是下列两个数据:1.10 g·cm-3,相当于含溶质质量分数为14.35%的硫酸、1.28 g·cm-3,相当于含溶质质量分数为36.87%的硫酸,请指出ρ1、ρ2分别对应于哪个数据?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com