
【题目】下列说法正确的是
A. 干燥氯气能使pH试纸先变红后褪色
B. SO2能使溴水褪色,体现了SO2的漂白性
C. 硅酸钠的溶液中通入二氧化碳会产生沉淀
D. 固体Na2CO3比固体NaHCO3稳定,相同条件下在水中NaHCO3比Na2CO3溶解度更大
科目:高中化学 来源: 题型:
【题目】将5.1g镁铝合金溶于70ml4mol/L硫酸中,当合金完全溶解后,再加入70ml8mol/L的NaOH溶液,得沉淀的质量为13.6g,则加入硫酸时,产生H2的物质的量为
A. 0.2mol B. 0.25mol C. 0.3mol D. 0.35mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质分类的叙述错误的是
A. 饱和食盐水属于混合物
B. Na2CO3即属于钠盐又属于碳酸盐
C. CuSO4·5H2O属于混合物
D. 纯净物一般可分成单质和化合物两类
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃、101 kPa下,1g氢气燃烧生成液态水,放出142.9kJ热量,能表示H2燃烧热的热化学方程式为( )
A.2H2(g)+O2(g)==2H2O(1) △H=―571.6kJ/mol![]()
B.2H2(g)+O2(g)==2H2O(1) △H=+571.6kJ/mol
C.H2(g)+![]() O2(g)==H2O(g) △H=―285.8kJ/mol
O2(g)==H2O(g) △H=―285.8kJ/mol
D.H2(g)+![]() O2(g)==H2O(1) △H=―285.8kJ/mol
O2(g)==H2O(1) △H=―285.8kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的化合物在生产生活中广泛存在。
(1)①可通过反应:NH3(g)+ Cl2(g)=NH2Cl(g)+ HCl(g)制备氯胺,己知部分化学键的键能:
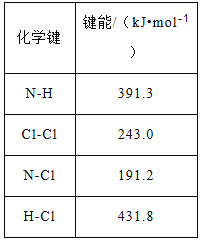
则上述反应的△H=______________。
② NH2Cl与水反应生成强氧化性的物质,可作长效缓释消毒剂,该反应的化学方程式为:_________________。
(2)用焦炭还原NO的反应为:2NO(g)+C(s) ![]() N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容恒温(反应温度分别为400 ℃、400 ℃、T ℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t 的变化情况如下表所示:
N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容恒温(反应温度分别为400 ℃、400 ℃、T ℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t 的变化情况如下表所示:
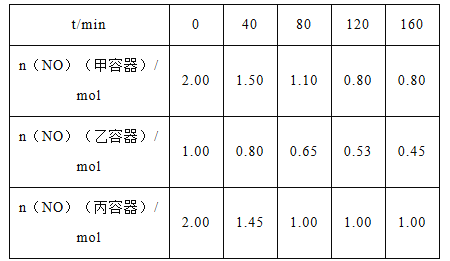
①该反应为________(填“放热”或“吸热”)反应
②乙容器在200min达到平衡状态,则0~200 min内用NO的浓度变化表示的平均反应速率v(NO)=_________。
(3)用焦炭还原NO2的反应为:2NO2(g)+2C(s)![]() N2(g)+2CO2(g),在恒温条件下,1 mol NO2和足量C发生该反应,平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
N2(g)+2CO2(g),在恒温条件下,1 mol NO2和足量C发生该反应,平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
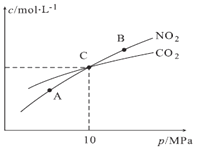
A、B两点的浓度平衡常数关系:Kc(A)________Kc(B)(填“< ”或“> ”或“=”)。
A、B、C三点中NO2的转化率最高的是:__________(填“A”或“B”或“C”)点.
计算C点时该反应的压强平衡常数:Kp(C)=____________(Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列氧化还原反应中,水既不作氧化剂又不作还原剂的是()
①2Na+2H2O=2NaOH+H2↑
②2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
③2F2+2H2O=O2+4HF
④3NO2+H2O=2HNO3+NO
⑤NaH+H2O=NaOH+H2↑
⑥2Na2O2+2H2O=4NaOH+O2↑
A. ③④⑥ B. ②③⑤ C. ①②③⑤ D. ④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
Ⅰ.下表是某食品包装上的说明,表中列出了部分配料。请回答:

配料中,富含维生素的是_________(填序号,下同),属于调味剂的是__________,属于防腐剂的是 富含油脂的是___________。
Ⅱ.化学与生活密切相关。请判断下列说法是否正确(填“对”或“错”)。
(1)很多水果具有酸味,因此在生理上称为酸性食物。
(2)纤维素作为人类的营养物质,在人体内具有重要的生理功能。
(3)钢铁在潮湿的空气中被腐蚀,主要是在钢铁表面发生了电化学腐蚀的原因。
(4)装饰材料挥发出来的有机物如甲醛、苯等,是室内空气污染的重要来源之一。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组的同学在实验室中用含有铝、铁、铜的废弃合金为主要原料制取硫酸铝溶液、硝酸铜晶体和无水氯化铁,其实验流程如下图所示。
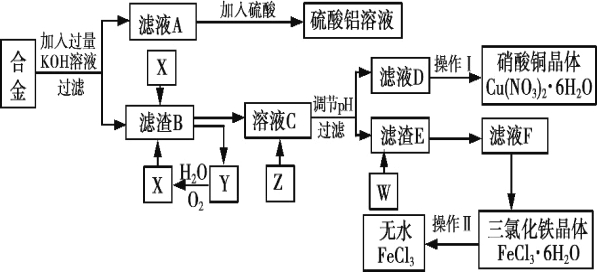
已知:Fe3+沉淀的pH范围为1.9~3.2;Cu2+沉淀的pH范围为4.7~6.7。
请回答下列问题:
(1)写出向合金中加入KOH溶液后所发生反应的离子方程式:__________________,若在该反应中转移0.6NA的电子,则获得标准状况下的气体体积为________L。
(2)下列物质中可作为试剂Z的是_______(填序号)。
A.铜粉 B.氨水 C.氧化铜
加入Z后,调节溶液的pH范围应为________________。
(3)实验操作Ⅰ的顺序依次为____________(填序号)。
A.蒸发浓缩 B.过滤 C.冷却结晶
(4)写出滤渣E与W反应的化学方程式______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com