
| A、Ka=-Kh |
| B、Ka=Kh-1 |
| C、Ka?Kh=Kw |
| D、Ka?Kw=Kh |
| [H+][A-] |
| [HA] |
| [HA][OH-] |
| [A-] |
| [H+][A-] |
| [HA] |
| [HA][OH-] |
| [A-] |
| [H+][A-] |
| [HA] |
| [HA][OH-] |
| [A-] |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、氢气与氮气能够缓慢地反应生成氨气,使用合适的催化剂可以提高化学反应速率 |
| B、等质量的锌粉和锌片与相同体积、相同浓度的盐酸反应,反应速率相等 |
| C、用铁片与硫酸制备氢气时,浓硫酸可以加快产生氢气的速率 |
| D、增大反应CO2(g)+H2(g)═CO(g)+H2O(g)的压强,反应速率不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32- |
| B、加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42? |
| C、加入盐酸无现象,再加氯化钡溶液有白色沉淀生成,原溶液一定有硫酸根离子 |
| D、加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、FeCl2 |
| B、AgNO3 |
| C、NaOH |
| D、AlCl3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HCN溶液 |
| B、HF溶液 |
| C、CH3COOH溶液 |
| D、HNO2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| 450℃ |
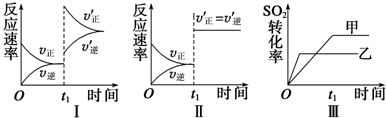
| A、图Ⅰ表示的是t1时刻增大O2的浓度对反应速率的影响 |
| B、图Ⅱ表示的是t1时刻加入催化剂后对反应速率的影响 |
| C、图Ⅲ表示的是催化剂对平衡的影响,且甲的催化效率比乙高 |
| D、图Ⅲ表示的是压强对化学平衡的影响,且乙的压强较高 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 .2009年1月11日,国际人权组织--人权观察曾在其报告中指责以色列在加沙人口稠密地区使用了违禁武器.该组织在报告中指出,以军在轰炸和炮击加沙地区时使用了白磷炸弹.下列说法不正确的是( )
.2009年1月11日,国际人权组织--人权观察曾在其报告中指责以色列在加沙人口稠密地区使用了违禁武器.该组织在报告中指出,以军在轰炸和炮击加沙地区时使用了白磷炸弹.下列说法不正确的是( )| A、白磷着火点低,在空气中可自燃 |
| B、白磷、红磷为同素异形体 |
| C、31 g白磷中,含P-P键1.5 mol |
| D、已知P4(白磷)+3O2(g)═2P2O3(s)△H=-Q kJ?mol-1,则白磷的燃烧热为Q kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氧化镁是优质耐高温材料 |
| B、家庭用的铝锅不宜用碱水洗涤,也不宜用来蒸煮酸的食物 |
| C、常温下,铝片放入浓硝酸中发生剧烈反应 |
| D、镁可用于制造照明弹 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com