
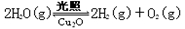 纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的四种方法:
纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的四种方法:
| 方法a | 用炭粉在高温条件下还原CuO |
| 方法b | 用葡萄糖还原新制的Cu(OH)2制备Cu2O; |
| 方法c |
|
| 方法d | 用肼(N2H4)还原新制的Cu(OH)2 |
(1)已知:2Cu(s)+1/2O2(g)=Cu2O(s);△H = -169kJ·mol-1
C(s)+1/2O2(g)=CO(g);△H = -110.5kJ·mol-1
Cu(s)+1/2O2(g)=CuO(s);△H = -157kJ·mol-1
则方法a发生的热化学方程式是:
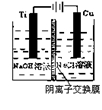
(2)方法c采用离子交换膜控制电解液中OH-的浓度而制备纳米 Cu2O,装置
如右图所示:该电池的阳极反应式为 钛极附近的pH值
(增大、减小、不变)
(3)方法d为加热条件下用液态肼(N2H4)还原新制Cu(OH)2来制 备纳米级Cu2O,
备纳米级Cu2O,
同时放出N2。该制法的化学方程式为 
(4)在相同的密闭容器中,用以上方法制得的三种Cu2O分别进行催化分解水的实验:  △H>0。水蒸气的浓度随时间t变化如下表所示。
△H>0。水蒸气的浓度随时间t变化如下表所示。
| 序号 |
| 0 | 10 | 20 | 30 | 40 | 50 |
| ① | T1 | 0.050[Co | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
| ② | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
| ③ | T2 | 0.10 | 0.094 | 0.0 | 0.090 | 0.090 | 0.090 |
下列叙述正确的是 (填字母)。
A.实验的温度:T2<T1 B.实验②比实验①所用的催化剂催化效率高
C.实验①前20 min的平均反应速率 v(H2)=7×10-5 mol·L-1 min-1
 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:
向溶液X中持续通入气体Y,会产生“浑浊→澄清”现象的是( )
A.X:漂白粉溶液 Y:二氧化硫
B.X:硝酸钡溶液 Y:二氧化硫
C.X:氯化铝溶液 Y:氨气
D.X:偏铝酸钠溶液 Y:二氧化氮
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学实验基本操作中正确的是( )
A.分液时,碘的四氯化碳溶液从分液漏斗下口放出,水层从上口倒出
B.蒸馏时,水从冷凝管上部通入,从下部流出
C.滴定时,左手控制滴定管活塞,右手握持锥形瓶,边滴边振荡并平视滴定管内液面
D.称量时,将纯碱放在称量纸上置于托盘天平的右盘,将砝码放在托盘天平的左盘
查看答案和解析>>
科目:高中化学 来源: 题型:
对室温下等pH、等体积的醋酸和盐酸两种溶液分别采取下列 措施,有关叙述正确的是
措施,有关叙述正确的是
A.加适量的醋酸钠晶体后,两溶液的pH均增大
B.加入足量的苏打固体充分反应后,两溶液中产生的CO2一样多
C.加水稀释2倍后,两溶液的pH均减小
D.加足量的锌充分反应后,盐酸中产生的氢气速率快
查看答案和解析>>
科目:高中化学 来源: 题型:
利用右图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产。下列说法
中正确的是( )
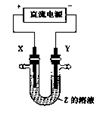
A.氯碱 工业中,X、Y均为石墨,X附近能得到氢氧化钠
工业中,X、Y均为石墨,X附近能得到氢氧化钠
B.铜的精炼中,X是纯铜,Y是粗铜,Z是CuSO4
C.电镀工业中,X是待镀金属,Y是镀层金属
D.外加电流的阴极保护法中,Y是待保护金属
查看答案和解析>>
科目:高中化学 来源: 题型:
下述对乙烯和聚乙烯的描述不正确的是 ( )
A.乙烯是纯净物,常温下为气态,聚乙烯为固态,是混合物
B.乙烯和聚乙烯性质均活泼,易发生加成反应
C.取等质量的乙烯和聚乙烯完全燃烧后,生成的CO2和H2O的质量分别相等
D.取等物质的量的乙烯和聚乙烯,完全燃烧后生成的CO2和H2O的物质的量分别相等
查看答案和解析>>
科目:高中化学 来源: 题型:
有关石油的分馏和煤的干馏两种变化,下列叙述错误的是 ( )
A.加热的温度二者不同
B.获得的产品二者不同
C.前者是物理变化,后者是化学变化
D.前者不需要隔绝空气,后者需隔绝空气
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、M、N是短周期主族元素,且原子序数依次增大。已知X原子的最外层电子数是电子层数的3倍,X、M同主族,Y原子在短周期主族元素中原子半径最大。下列说法正确的是
A.M与X的化合物对应的水化物一定是强酸
B.Y2X和Y2X2中化学键类型相同,阴、阳离子的个数比相同
C.气态氢化物的热稳定性:M > N
D.离子半径r:r(X2-)> r(Y+)
查看答案和解析>>
科目:高中化学 来源: 题型:
在300 mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni(s)+4CO(g)  Ni(CO)4(g),已知该反应平衡常数与温度的关系如下:
Ni(CO)4(g),已知该反应平衡常数与温度的关系如下:
| 温度/℃ | 25 | 80 | 230 |
| 平衡常数 | 5×104 | 2 | 1.9×10-5 |
下列说法不正确的是( )
A.上述生成Ni(CO)4(g)的反应为放热反应
B.25 ℃时反应Ni(CO)4(g)  Ni(s)+4CO(g)的平衡常数为2×10-5
Ni(s)+4CO(g)的平衡常数为2×10-5
C.在80 ℃时,测得某时刻,Ni(CO)4、CO浓度均为0.5 mol/L,则此时v(正)>v(逆)
D.80 ℃达到平衡时,测得n(CO)=0.3 mol,则Ni(CO)4的平衡浓度为2 mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com