
将氮气、氢气的混合气体分别充入甲、乙、丙三个容器中进行合成氨反应,经过一段时间后,反应速率为:甲:v (H2)=3mol/(L· min);乙:v (N2) =2mol/(L·min);丙: v (NH3)= 1mol/(L·min),则这段时间内三个容器中反应速率由大到小的顺序是 。
科目:高中化学 来源: 题型:阅读理解
| ||
| ||
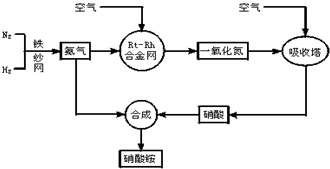
| C4(NO)?C6(H2O) |
| C4(NH3)?C5(O2) |
| C4(NO)?C6(H2O) |
| C4(NH3)?C5(O2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| T/K | T1 | 573 | T2 |
| K | 1.00×107 | 2.45×105 | 1.88×103 |
| 1 |
| 7 |
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
反应前: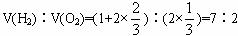
反应后: ![]()
A.2∶7 B.7∶5 C.4∶5 D.8∶1
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| T/K | T1 | 573 | T2 |
| K | 1.00×107 | 2.45×105 | 1.88×103 |
| 1 |
| 7 |
| ||
查看答案和解析>>
科目:高中化学 来源:2011-2012学年江苏省南通市如皋市高三(上)期中化学试卷(解析版) 题型:填空题
| T/K | T1 | 573 | T2 |
| K | 1.00×107 | 2.45×105 | 1.88×103 |
 ,此时N2的转化率为 .
,此时N2的转化率为 .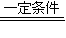 4NO+6H2O 4NO+3O2+2H2O=4HNO3
4NO+6H2O 4NO+3O2+2H2O=4HNO3查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com