
【题目】分子式为C7H16的烷烃中,含有3个甲基的同分异构体的数目为( )
A.2个 B.3个 C.4个 D.5个
科目:高中化学 来源: 题型:
【题目】某胶体在电泳时,它的胶粒向阴极移动。在这种胶体中分别加入下列物质:
①淀粉溶液②硫酸镁溶液③硅酸胶体④氢氧化铁胶体,不会发生聚沉的是
A.①③B.①④C.②③D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D四种短周期元素的核电荷数依次增大。A原子s轨道电子数是p轨道电子数的两倍,C原子的L能层中有两对成对电子,C、D同主族。 E、F是第四周期元素,且E位于周期表中ds区, F原子核外有33种不同运动状态的电子。根据以上信息用相应的元素符号填空:
(1)E+核外电子排布式为 ,FC43-离子的空间构型为 ,与其互为等电子体的一种有机分子为 (填化学式)。
(2)B元素所在周期第一电离能最大的元素是 (填元素符号)。
(3)D所在周期元素最高价氧化物对应的水化物中,酸性最强的是 (填化学式);能导电的A单质与B、D、E的单质形成的晶体相比较,熔点由高到低的排列顺序是 (填化学式)。
(4)已知EDC4溶液中滴入氨基乙酸钠(H2N—CH2—COONa)即可得到配合物A。其结构如图所示:
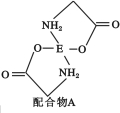
① 配合物A中碳原子的轨道杂化类型为 。
② 1 mol氨基乙酸钠(H2N—CH2—COONa)含有σ键的数目为 。
(5)化合物F2C3常用于标定未知浓度的酸性KMnO4溶液,反应生成F的最高价含氧酸,该反应的离子方程式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将等物质的量的A、B混合于2L密闭容器中发生如下反应:3A(g)+B(g) ![]() xC(g)+2D(g),4min时测得D的浓度为0.4mol/L,c(A):c(B)=3:5,C的平均反应速率是0.1mol/(L.min),列式计算:
xC(g)+2D(g),4min时测得D的浓度为0.4mol/L,c(A):c(B)=3:5,C的平均反应速率是0.1mol/(L.min),列式计算:
(1)x=__________;
(2)B在这4min内的平均反应速率__________;
(3)此时A的浓度及反应开始前容器中A、B的物质的量__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)有下列几组物质,请将序号填入下列空格内:
A、CH2=CH-COOH和油酸(C17H33COOH) B、12C60和石墨
C、![]() 和
和![]() D、35Cl和37Cl E、乙醇和乙二醇
D、35Cl和37Cl E、乙醇和乙二醇
①互为同位素的是 ;
②互为同系物的是 ;
③互为同素异形体的是 ;
④互为同分异构体的是 ;
⑤既不是同系物,又不是同分异构体,也不是同素异形体,但可看成是同一类物质的是 。
(2)请写出下列反应的化学方程式:
①由丙烯制取聚丙烯: ;;
②丙氨酸缩聚形成多肽: ;
③淀粉水解: ;
④丙醛与新制的氢氧化铜悬浊液反应: ;
(3)用一种试剂将下列各组物质鉴别开,写出其名称。
①![]() 和
和![]() : ;
: ;
② ![]() ,
,![]() 和C6H12(己烯): ;
和C6H12(己烯): ;
③ ![]() ,CCl4和乙醇 。
,CCl4和乙醇 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究人员发现了一种“水”电池,其总反应为:5MnO2 +2Ag+2NaCl =Na2 Mn5O10 +2AgCl。如图用“水”电池为电源电解NaCI溶液的实验中,X电极上有无色气体逸出。下列有关分析正确的是( )

A.I为负极,其电极反应式为Ag十Cl-+e-=AgCl
B.“水”电池内Na+不断向负极作定向移动
C.每转移1mole-,U型管中消耗0.5mol H2O
D.开始时U型管中Y极附近pH逐渐增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丰富的CO2完全可以作为新碳源,解决当前应用最广泛的碳源(石油和天然气)到本世纪中叶将枯竭的危机。
(1)目前工业上有一种方法是用CO2和H2在230℃催化剂条件下转化生成甲醇(CH3OH)蒸汽和水蒸气CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)。下图表示恒压容器中充入1mol CO2和3 mol H2,转化率达50%时的能量变化示意图。写出该反应的热化学方程式: 。
CH3OH(g)+H2O(g)。下图表示恒压容器中充入1mol CO2和3 mol H2,转化率达50%时的能量变化示意图。写出该反应的热化学方程式: 。

(2)另外工业上还可用CO和H2制备甲醇。 反应为CO(g)+2H2(g)![]() CH3OH(g),
CH3OH(g),
某温度下,在容积为2L的恒容密闭容器中进行该反应,其相关数据见下图:

① t min至2t min时速率变化的原因可能是 ;
② 3t min时对反应体系采取了一个措施,至4t min时CO的物质的量为0.5mol,请完成上图CO的曲线。
(3)CO2在一定条件下,还可以与H2合成二甲醚:
2CO2(g)+6H2(g)![]() CH3OCH3(g)+3H2O(g)。
CH3OCH3(g)+3H2O(g)。
将2.5 mol H2与b mol CO2置于容积为1 L的密闭容器中,发生上述反应,达到平衡状态时,测得实验数据如下表:

① 降温时,上述平衡向_________方向移动(填“正反应”或“逆反应”)。
②表中x、y的大小关系为_________。
A.x=y B.x>y C.x<y D.无法判断
③表中x、y、z、w对应的平衡常数分别为Kx、Ky、Kz、Kw,它们之间的大小关系为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向某密闭容器中充入1 mol CO和2 mol H2O(g),发生反应:CO+H2O(g)![]() CO2+H2。当反应达到平衡时,CO的体积分数为x。若维持容器的体积和温度不变,起始物质按下列四种配比充入该容器中,达到平衡时CO的体积分数大于x的是( )
CO2+H2。当反应达到平衡时,CO的体积分数为x。若维持容器的体积和温度不变,起始物质按下列四种配比充入该容器中,达到平衡时CO的体积分数大于x的是( )
A. 0.5 mol CO+2 mol H2O(g)+1 mol CO2+1 mol H2
B. 1 mol CO+1 mol H2O(g)+1 mol CO2+1 mol H2
C. 0.5 mol CO+1.5 mol H2O(g)+0.4 mol CO2+0.4 mol H2
D. 0.5 mol CO+1.5 mol H2O(g)+0.5 mol CO2+0.5 mol H2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com