
 2NH3(g)△H
2NH3(g)△H| A.3v(H2)正=2v(NH3)逆 |
| B.单位时间内生成n mol N2的同时生成2n molNH3 |
| C.混合气体的密度不再改变 |
| D.容器内压强不随时间的变化而变化 |
| 实验编号 | T(℃) | n (N2)/n(H2) | P(MPa) | 平衡时NH3百分含量 |
| ⅰ | 450 | 1/3 | 1 | |
| ⅱ | ① | 1/3 | ② | |
| ⅲ | 480 | 1/3 | 10 | |
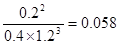 。正反应是放热反应,升高温度,平衡向逆反应方向移动,平衡常数减小。
。正反应是放热反应,升高温度,平衡向逆反应方向移动,平衡常数减小。

 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:单选题
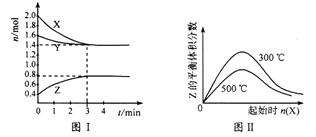
A.该反应的化学方程式为: 2X(g) + Y(g) 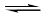 2Z(g) 2Z(g) |
| B.反应进行的前3min内,用X表示的平均反应速率v(x)=0.067mol/(L·min) |
| C.由图II可知,其他条件不变,增大X的量时Y的转化率先增大后减小 |
| D.其他条件不变,升髙温度,平衡逆向移动 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CO2(g)+ H2(g) ;△H<0。在850℃时,平衡常数K=1。
CO2(g)+ H2(g) ;△H<0。在850℃时,平衡常数K=1。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2SO3。请填写下列空白:
2SO3。请填写下列空白: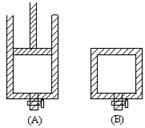
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
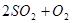
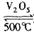
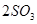 。如果反应在密闭容器中进行,下列说法错误的是
。如果反应在密闭容器中进行,下列说法错误的是A.当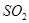 的物质的量不再改变时,该反应达到了平衡状态 的物质的量不再改变时,该反应达到了平衡状态 |
B.达到平衡时,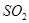 的浓度与 的浓度与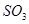 的浓度一定相等 的浓度一定相等 |
C.在给定条件下达平衡时,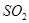 的转化率达到了最大 的转化率达到了最大 |
D.使用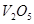 催化剂是为了加快反应速率,提高生产效率 催化剂是为了加快反应速率,提高生产效率 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 Z(g) ⊿H>0。经60s达到平衡,生成0.3mol Z。下列说法正确的是
Z(g) ⊿H>0。经60s达到平衡,生成0.3mol Z。下列说法正确的是| A.以Y浓度变化表示的反应速率为0.0005mol·L-1·s-1 |
| B.以X浓度变化表示的反应速率为0.0005mol·L-1·s-1 |
| C.若单位时间内生成a mol Y的同时,生成2a mol X,则反应达到平衡状态 |
| D.若升高温度,正反应速率增大,逆反应速率减小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 H2(g)+CO(g)。
H2(g)+CO(g)。 CH3OH(g)。一定条件下,向体积为1 L的密闭容器中充入1 mol CO和3 mol H2,反应达到平衡状态时,CO的平衡转化率为75%。
CH3OH(g)。一定条件下,向体积为1 L的密闭容器中充入1 mol CO和3 mol H2,反应达到平衡状态时,CO的平衡转化率为75%。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2C(g) △H<0
2C(g) △H<0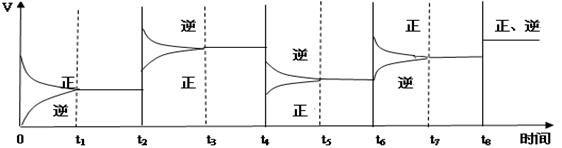
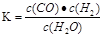
| A.容器中气体的平均相对分子质量不随时间而变化 |
| B.υ正(H2O)=υ逆(H2) |
| C.容器中气体的密度不随时间而变化 |
| D.容器中总的物质的量不随时间而变化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2C在不同温度下的平衡常数:
2C在不同温度下的平衡常数:| 温度 | 500C | 800C |
| K | 100 | 400 |
 A+B的平衡常数为0.05,可推知t的范围是( )
A+B的平衡常数为0.05,可推知t的范围是( )查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com