
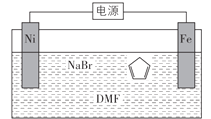
【题目】环戊二烯可用于制备二茂铁(Fe(C5H5)2,结构简式为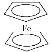 ),后者广泛应用于航天、化工等领域中。二茂铁的电化学制备原理如图所示,其中电解液为溶解有溴化钠(电解质)和环戊二烯的DMF溶液(DMF为惰性有机溶剂)。下列说法错误的是( )
),后者广泛应用于航天、化工等领域中。二茂铁的电化学制备原理如图所示,其中电解液为溶解有溴化钠(电解质)和环戊二烯的DMF溶液(DMF为惰性有机溶剂)。下列说法错误的是( )
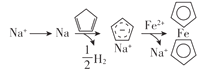
A.制备二茂铁总反应为:Fe+2![]() =
=![]() +H2↑
+H2↑
B.电解制备需要在无水条件下进行
C.Ni电极与电源负极连接
D.阳极电极反应为:2Br--2e-=Br2
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】(I)在水溶液中橙红色的Cr2O72--与黄色的CrO42--有下列平衡关系:Cr2O72--+H 2O![]() 2CrO42--+2H+现将一定量的K2Cr2O7溶于水配成稀溶液,溶液呈橙色。
2CrO42--+2H+现将一定量的K2Cr2O7溶于水配成稀溶液,溶液呈橙色。
(1)向上述溶液中加入浓硫酸溶液,溶液呈__________色,因为_____________________。
(2)向原溶液中加入Ba(NO3)2溶液(已知BaCrO4为黄色沉淀),则平衡向__________方向移动(正或逆),溶液颜色将__________(加深或变浅)。
(II)工业上有一种用CO2生产甲醇燃料的方法:
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH=-49.0 kJ/mol
CH3OH(g)+H2O(g) ΔH=-49.0 kJ/mol
某实验中将6 mol CO2和8 mol H2充入2 L的密闭容器中,测得H2的物质的量随时间变化如图曲线 (甲)所示。请完成下列问题:
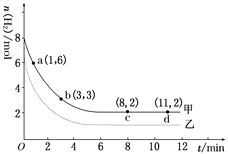
(1)a点正反应速率________逆反应速率(填“>”、“<”或“=”)。
(2)若仅改变某一实验条件再进行一次实验,测得H2的物质的量随时间变化如图中虚线(乙)所示,曲线(乙)对应改变的实验条件可以是________(填序号)。
a.加催化剂 b.增大压强 c.升高温度 d.增大H2浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一)A、B、C、D、E、X是中学常见的无机物,存在如图转化关系(部分生成物和反应条件略去)。
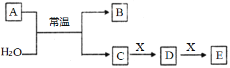
(1)若A为常见的金属单质,且其焰色反应呈黄色,X能使品红溶液褪色,写出C和E反应的离子方程式:___。
(2)若A为短周期元素组成的单质,该元素的最高价氧化物的水化物酸性最强,则X可能为__(填字母)。
a.NaHCO3 b.Na2CO3 c.Al(OH)3 d.NaAlO2
(3)若A为淡黄色粉末,则A的电子式为___。若X为一种最常见的造成温室效应的气体。则鉴别等浓度的D、E两种溶液,可选择的试剂为___。(填字母)
a.盐酸 b.CaCl2溶液 c.氨水 d.澄清石灰水
(二)工业废水中仅含下表离子中的5种(不考虑水的电离及离子的水解),且各种离子的物质的量浓度均为0.1mol![]() L-1。
L-1。
阳离子 | K+、Cu2+、Fe3+、Al3+、Fe2+ |
阴离子 | Cl-、CO32-、NO3-、SO42-、SiO32- |
某同学欲探究该废水的组成,进行了如下实验:
Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察)。
Ⅱ.取少量溶液,加入KSCN溶液无明显变化。
Ⅲ.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变。
Ⅳ.向Ⅲ 中所得溶液中加入BaCl2溶液,有白色沉淀生成。
请回答下列问题:
(1)甲同学最终确定原溶液中所含阳离子有___,阴离子是有___。(写离子符号)
(2)Ⅲ中加入少量盐酸生成无色气体的离子方程式为___。
(3)另取100mL原溶液,加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,得到的固体的质量为__g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化过程中,熵变小于0的是
A.H2O(s)→H2O(l)→H2O(g)
B.N2(g)+3H2(g)![]() 2NH3(g)
2NH3(g)
C.NaOH(s)=Na+(aq)+OH-(aq)
D.2NaHCO3(s)![]() Na2CO3(s)+CO2(g)+H2O(g)
Na2CO3(s)+CO2(g)+H2O(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向![]() 和
和![]() 的混合溶液中不断加入
的混合溶液中不断加入![]() 溶液,得到沉淀的物质的量与加入
溶液,得到沉淀的物质的量与加入![]() 溶液体积的关系如图所示。下列说法不正确的是( )
溶液体积的关系如图所示。下列说法不正确的是( )
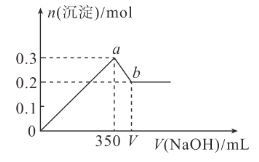
A.![]()
B.![]() 溶液的物质的量浓度为
溶液的物质的量浓度为![]()
C.![]() 与
与![]() 的物质的量浓度之比为
的物质的量浓度之比为![]()
D.![]() 段反应的离子方程式为
段反应的离子方程式为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)现有![]() 某气体(由双原子分子构成),其摩尔质量为
某气体(由双原子分子构成),其摩尔质量为![]() ,阿伏加德罗常数用
,阿伏加德罗常数用![]() 表示,试求
表示,试求
①该气体在标准状况下的体积为____![]() 。
。
②该气体所含原子数为____。
(2)用双线桥表示铜与浓硫酸反应的电子转移方向和数目:__________________
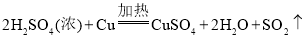
当有![]() 被还原时,转移电子的物质的量为____
被还原时,转移电子的物质的量为____![]() ,生成标准状况下
,生成标准状况下![]() 的体积为___
的体积为___![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖授予约翰·古德伊纳夫、斯坦利·惠廷厄姆和吉野彰三位科学家,以表彰他们在锂电池领域所做出的巨大贡献。请回答下列问题:
(1)LiCoO2、LiFePO4常用作锂离子电池的正极材料。基态Co原子核外电子排布式为___,基态磷原子中,电子占据的最高能层符号为___;该能层能量最高的电子云在空间有___个伸展方向,原子轨道呈___形。
(2)[Co(NO3-)4]2-中Co2+的配位数为4,配体中N的杂化方式为__,该配离子中各元素的第一电离能由小到大的顺序为___(填元素符号),1mol该配离子中含σ键数目为___NA。
(3)LiFePO4属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如图所示:
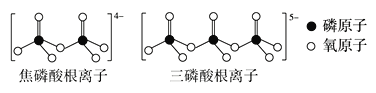
这类磷酸根离子的化学式可用通式表示为___(用n代表P原子数)。
(4)钴蓝晶体结构如图,该立方晶胞由4个I型和4个Ⅱ型小立方体构成,其化学式为___,晶体中Al3+占据O2-形成的___(填“四面体空隙”或“八面体空隙”)。NA为阿伏加德罗常数的值,钴蓝晶体的密度为___g·cm-3(列计算式)。
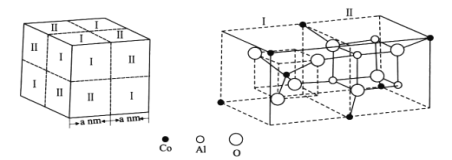
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“重油—氧气—熔融碳酸钠”燃料电池装置如图所示。下列说法不正确的是( )
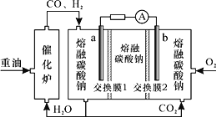
A.b为电池的正极
B.放电过程中,电子由电极a经导线流向电极b
C.该电池工作时,CO32-经交换膜2移向b极
D.H2参与的电极反应为:H2-2e-+CO32-=H2O+CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向 Fe 和 Fe2O3 组成的 3.84g 混合物中加入 120mL 某浓度的盐酸,恰好完全反应,生成 672mL H2(标准状况下);向反应后的溶液中滴加几滴 KSCN 溶液,溶液无明显变化。(结果保留三位有效数字)
(1)原混合物中Fe 的质量为____________g.
(2)所用盐酸的物质的量浓度为____________mol/L.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com