
| m |
| M |
| V |
| Vm |
| 13.44L |
| 22.4L/mol |
| 5.6g |
| 28g/mol |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、盐酸、硫酸 |
| B、盐酸、NaOH溶液 |
| C、氨水、硫酸 |
| D、氨水、NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、42He原子核内有4个质子 |
| B、42He的最外层电子数为2 |
| C、32He原子核内含有3个质子 |
| D、32He与42He互为同位素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HCl、CuSO4、Mg(NO3)2、KOH |
| B、NaBr、AgNO3、HCl、Na2CO3 |
| C、H2SO4、NaCl、Na2SO4、Na2CO3 |
| D、NaOH、MgSO4、Na2CO3、KHSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
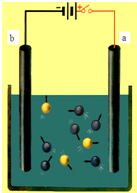 如图是电解氯化铜溶液的装置,其a、b为石墨电极,则下列有关的判断中正确的是( )
如图是电解氯化铜溶液的装置,其a、b为石墨电极,则下列有关的判断中正确的是( )| A、a为正极,b为负极 |
| B、a极上发生还原反应 |
| C、电解过程中,b电极上有铜析出 |
| D、电解过程中,氯离子浓度保持不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaOH、H2SO4、Na2SO4 |
| B、NaOH、AgNO3、H2SO4 |
| C、HCl、CuBr2、Ba(OH)2 |
| D、KBr、H2SO4、Ba(OH)2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com