
| A. | 上述过程中,最终被还原的是NO3- | |
| B. | 从上述过程中可以得出结论,氧化性:HNO3>Fe3+>稀H2SO4 | |
| C. | 假设通入的SO2完全反应,则同温同压下,SO2和逸出气体的体积为1:1 | |
| D. | 上述过程中,会产生一种无色的难溶于水的气体 |
分析 将SO2通入Fe(NO3)3溶液中,溶液由棕黄色变为浅绿色,发生氧化还原反应生成亚铁离子和硫酸根离子,发生离子反应为SO2+2Fe3++2H2O=SO42-+2Fe2++4H+;立即又变为棕黄色,发生亚铁离子与硝酸根离子的氧化还原反应,生成铁离子,离子反应为3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,以此解答该题.
解答 解:A、溶液由黄色变为浅绿色,但立即又变为黄色,三价铁离子变为亚铁离子,后又被氧化为三价铁离子,所以最终被还原的是NO3-,故A正确;
B、由溶液有棕色变为浅绿色,说明三价铁的氧化性强于稀硫酸,但在硝酸存在的前提下立即又变成棕黄色,说明亚铁迅速被氧化成铁离子,故硝酸的氧化性强三价铁,综上所述氧化性:HNO3>Fe3+>稀硫酸,故B正确;
C、上述过程中,最终被还原的是NO3-,故相当于二氧化硫与硝酸根离子之间的氧化还原,3SO2~2NO3-,之比为3:2,故C错误;
D、硝酸根离子和二氧化硫被氧后产生的氢离子构成强氧化性体系,氧化亚铁时生成无色的一氧化氮气体,故D正确;
故选C.
点评 本题比较综合,涉及氧化还原、离子反应方程式书写、化学反应的计算等,把握习题中的信息及发生的化学反应为解答的关键,较好的考查学生分析问题、解决问题的能力,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | CH4+2O2→CO2+2H2O | B. | CH2=CH2+Br2→CH2Br-CH2Br | ||
| C. | CH4+Cl2→CH3Cl+HCl | D. | 2CH3CH2OH+O2→2CH3CHO+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 失电子越多,还原性就越强,得电子越多,氧化性越强 | |
| B. | 金属单质在化学反应中一定作为还原剂,非金属单质在反应中可以作氧化剂 | |
| C. | 强电解质溶液的导电能力一定强,弱电解质溶液的导电能力一定弱 | |
| D. | 凡是强酸和强碱反应的离子方程式都可以用H++OH-=H2O表示 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将煤干馏制得煤焦油和焦炭 | |
| B. | 从海水中可以得到氯化镁,再加热分解可制金属镁 | |
| C. | 将石油裂解制得乙烯等化工原料 | |
| D. | 煤的气化主要反应是C(s)+H2O(g)$\frac{\underline{\;高温\;}}{\;}$CO(g)+H2(g) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化硼液态时能导电而固态时不导电 | |
| B. | 硼原子以sp3杂化 | |
| C. | 氯化硼分子属极性分子 | |
| D. | 氯化硼遇水蒸气会产生白雾 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ”,其结构如红十字协会的会徽,因此有人将它称为“红十字烷”,写出它的分子式C12H24,当它发生一氯取代物时,能生成2种沸点不同的产物.
”,其结构如红十字协会的会徽,因此有人将它称为“红十字烷”,写出它的分子式C12H24,当它发生一氯取代物时,能生成2种沸点不同的产物.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | C2H4和C5H6 | B. | 乙醇和二甲醚 | ||
| C. | 正丁烷和异戊烷 | D. | 一溴乙烷和二溴乙烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
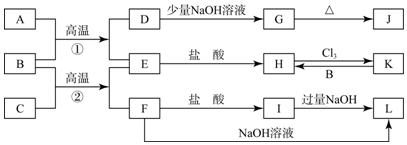
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com