
 ��
��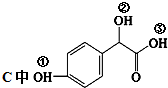 �١��ڡ���3��-OH��������ǿ������˳���ǣ�
�١��ڡ���3��-OH��������ǿ������˳���ǣ� ��
�� ��
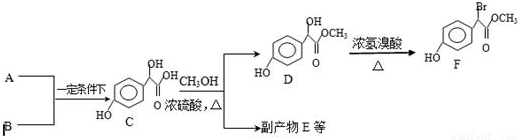
�� ���� A�ķ���ʽΪC2H2O3���ɷ���������Ӧ���Ҿ������ԣ�����ȩ�����Ȼ�����A��OHCCOOH��A��B��Ӧ����C������C�Ľṹ��֪B��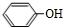 ��A+B��C�ķ�Ӧ�����Ǽӳɷ�Ӧ��
��A+B��C�ķ�Ӧ�����Ǽӳɷ�Ӧ��
C�ͼ״���Ũ���������������������·�Ӧ����D��E������E�ṹ��ʽ֪���÷�Ӧ��������Ӧ����EΪH2O��D���������ڼ��������·���ȡ����Ӧ����F���ݴ˷������
��� �⣺A�ķ���ʽΪC2H2O3���ɷ���������Ӧ���Ҿ������ԣ�����ȩ�����Ȼ�����A��OHCCOOH��A��B��Ӧ����C������C�Ľṹ��֪B�� ��A+B��C�ķ�Ӧ�����Ǽӳɷ�Ӧ��
��A+B��C�ķ�Ӧ�����Ǽӳɷ�Ӧ��
C�ͼ״���Ũ���������������������·�Ӧ����D��E������E�ṹ��ʽ֪���÷�Ӧ��������Ӧ����EΪH2O��D���������ڼ��������·���ȡ����Ӧ����F��
��1��ͨ�����Ϸ���֪��A��OHCCOOH��B�DZ��ӣ�A+B��C�ķ�Ӧ�����Ǽӳɷ�Ӧ����Ӧ����ʽΪ�� ��
��
�ʴ�Ϊ��ȩ�����Ȼ��� ��
��
��2���Ȼ�������ǿ�ڷ��ǻ������ǻ�������ǿ�ڴ��ǻ�����ǿ��˳��Ϊ���ۣ��٣��ڣ��ʴ�Ϊ���ۣ��٣��ڣ�
��3��C�����ǻ����Ȼ���2����C���Է���������Ӧ����������3����Ԫ���Ļ����C���Ӽ䴼�ǻ����Ȼ�����������Ӧ����EΪ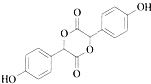 ��Ϊ�Գƽṹ����������4�ֻ�ѧ������ͬ��Hԭ�ӣ��ֱ�Ϊ������2�֡����ǻ���1�֡��Ǽ���1�֣�
��Ϊ�Գƽṹ����������4�ֻ�ѧ������ͬ��Hԭ�ӣ��ֱ�Ϊ������2�֡����ǻ���1�֡��Ǽ���1�֣�
�ʴ�Ϊ��4��
��4���Ա�D��F�Ľṹ����֪��ԭ��ȡ��-OHλ�ã�D��F�ķ�Ӧ�����ǣ�ȡ����Ӧ��F����ԭ�ӡ����ǻ��������������봼�γɵ������������������������Ʒ�Ӧ��1molF�������3mol NaOH��
F������ͬ���칹����ϣ�������һԪ�������ڱ�����ֻ��2��ȡ�����Ҵ��ڶ�λ������һ�����ǻ�������ȡ����Ϊ-CBr��CH3��COOH��-CH��CH2Br��COOH��-CH2CHBrCOOH��-CHBrCH2COOH�����ܵĽṹ��ʽΪ�� ��
��
�ʴ�Ϊ��ȡ����Ӧ��3�� ��
��
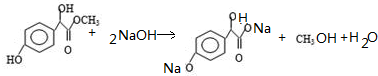
��5���÷�Ӧ����ʽΪ ��
��
�ʴ�Ϊ ��
��
���� ���⿼���л��ƶϣ�Ϊ��Ƶ���㣬��ȷ�����ż������ʹ�ϵ�ǽⱾ��ؼ�����������ʽṹ��ʽ�仯ȷ����Ӧ���ͣ���Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Cu�������S��ϼ��ȣ����յõ�CuS | |
| B�� | ������ͨ�������ʯ������Ư�� | |
| C�� | �����£���27 g A1Ͷ������18.4 mol•L-1�������У�����1.5 mol H2 | |
| D�� | ��SO2����ͨ��Ba��OH��2��Һ�У����յõ���ɫ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����£�pH��ͬ��NaOH��Һ��Ba��OH��2��Һ�У�ˮ�ĵ���̶Ȳ���ͬ | |
| B�� | NaHSO3��Һ������Ũ�ȴ�С˳��Ϊc��Na+����c��H+����c��HSO3-����c��SO32-����c��OH-�� | |
| C�� | �������2.24L��CO2ͨ��150mL 1mol•L-1NaOH��Һ�г�ַ�Ӧ�����Һ��2c��Na+��=3c��CO32-��+3c��HCO3-��+3c��H2CO3�� | |
| D�� | �����£�pH=3�Ķ�Ԫ����H2R��Һ��pH=11��NaOH��Һ��Ϻ����Һ��pH����7����Ӧ��Ļ��Һ��2c��R2-��+c��HR-����c��Na+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ۢ� | B�� | �ڢ� | C�� | �٢� | D�� | �٢� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ж���������Ϊ�������ͷ����� | |
| B�� | �����뺣���������γ�ͨ���뽺��������й� | |
| C�� | ��ʳ��ȥ��ˮ���е�ˮ��ʱ����������ˮ�ⷴӦ | |
| D�� | ú��ú���������仯���Ǹ�Ч����������ú����Ҫ;�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
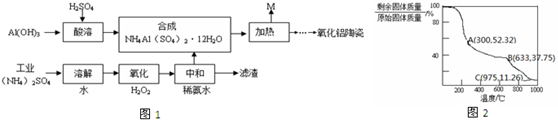
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com