
【题目】醋酸亚铬水合物[Cr(CH3COO)2]2·2H2O是一种氧气吸收剂,为红棕色晶体,易被氧化,微溶于乙醇,不溶于水和乙醚(易挥发的有机溶剂)。其制备装置及步骤如下:

①检查装置气密性,往三颈烧瓶中依次加入过量锌粉、适量CrCl3溶液。
②关闭k2打开k1,旋开分液漏斗的旋塞并控制好滴速。
③待三颈烧瓶内的溶液由深绿色(Cr3+)变为亮蓝色(Cr2+)时,把溶液转移到装置乙中,当出现大量红棕色晶体时,关闭分液漏斗的旋塞。
④将装置乙中混合物快速过滤、洗涤和干燥,称量得到2.76 g[Cr(CH3COO)2]2·2H2O。
(1)装置甲中连通管a的作用是______________________。
(2)三颈烧瓶中的Zn除了与盐酸生成H2外,发生的另一个反应的离子方程式为______________________。
(3)实验步骤③中溶液自动转移至装置乙中的实验操作为______________________。
(4)装置丙中导管口水封的目的是______________________。
(5)洗涤产品时,为了去除可溶性杂质和水分,下列试剂的正确使用顺序是________(填字母)。
a.乙醚 b.去氧冷的蒸馏水 c.无水乙醇
(6)若实验所取用的CrCl3溶液中含溶质3.17 g,则[Cr(CH3COO)2]2·2H2O(相对分子质量为376)的产率是______________________。
(7)一定条件下,[Cr(CH3COO)2]2·2H2O受热得到CO和CO2的混合气体,请设计实验检验这两种气体的存在________。
【答案】 保证分液漏斗中的液体顺利流下 2Cr3++Zn===2Cr2++Zn2+ 关闭k1,打开k2 防止空气进入装置乙氧化二价铬 bca 73.4% 混合气体通入澄清石灰水,变浑浊,说明混合气体中含有CO2;混合气体通过灼热的氧化铜,固体颜色由黑色变红色,说明混合体中含有CO
【解析】试题分析:(1)反应中有气体生成,会导致装置内压强增大,则装置甲中连通管a的作用是平衡压强,使分液漏斗中的液体顺利滴下。
(2) Cr3+具有氧化性,能氧化金属锌,则三颈瓶中的Zn除了与盐酸生成H2外,发生的另一个反应的离子方程式为Zn+2Cr3+=2Cr2++Zn2+。
(3)要实现步骤③中溶液自动转移至装置乙中,则可以借助于压强的变化来实现,由于三颈烧瓶中产生气体,所以实验操作为关闭K1,打开K2。
(4)由于空气中含有氧气,氧气能氧化二价铬,则装置丙中导管口水封的目的是防止空气进入装置乙氧化二价铬。
(5)由于醋酸亚铬水合物是一种氧气吸收剂,易被氧化,微溶于乙醇,不溶于水和乙醚(易挥发的有机溶剂),所以洗涤产品时,为了去除可溶性杂质和水分,正确使用顺序是先用去氧冷的蒸馏水,然后用乙醇,最后用乙醚,答案为bca。
(6)若实验所取用的CrCl3溶液中含溶质3.17 g,则根据原子守恒可知理论上得到产品的质量是![]() ,所以产率是
,所以产率是![]() 。
。
(7)二氧化碳能使澄清的石灰水变浑浊,所以可以用澄清石灰水检验二氧化碳;CO具有还原性,可以用氧化铜检验,即混合气体通入澄清石灰水,变浑浊,说明混合气体中含有CO2;混合气体通入灼热的CuO,固体颜色由黑色变红色,说明混合气体中有CO。


科目:高中化学 来源: 题型:
【题目】利用下列实验装置不能完成相应实验的是( )

A. 用装置①测量生成氧气的化学反应速率
B. 用装置②比较NaHCO3和Na2CO3的热稳定性
C. 装置③中分液漏斗内的液体可顺利加入蒸馏烧瓶
D. 装置④可实现制取CO2实验中的“即关即止,即开即用”的作用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏伽德罗常数,下列物质所含分子数最多的是( )
A.0.8 mol二氧化碳
B.标准状况下2.24L氨气
C.3.6 g水
D.含NA个氢分子的氢气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸镍[(CH3COO)2Ni]是一种重要的化工原料。一种以含镍废料(含NiS、Al2O3、FeO、CaO、SiO2)为原料,制取醋酸镍的工艺流程图如下:

相关离子生成氢氧化物的pH 和相关物质的溶解性如下表:
金属离子 | 开始沉淀的pH | 沉淀完全的pH | 物质 | 20℃时溶解性(H2O) |
Fe3+ | 1.1 | 3.2 | CaSO4 | 微溶 |
Fe2+ | 5.8 | 8.8 | NiF | 可溶 |
Al3+ | 3.0 | 5.0 | CaF2 | 难溶 |
Ni2+ | 6.7 | 9.5 | NiCO3 | Ksp=9.60×10-6 |
(1)调节pH 步骤中,溶液pH的调节范围是________。
(2)滤渣1和滤渣3 主要成分的化学式分别是________、________。
(3)写出氧化步骤中加入H2O2 发生反应的离子方程式________。
(4)酸浸过程中,1molNiS失去6 NA个电子,同时生成两种无色有毒气体。写出该反应的化学方程式________。
(5)沉镍过程中,若c(Ni2+)=2.0 mol·L-1,欲使100 mL该滤液中的Ni2+沉淀完全[c(Ni2+)≤10-5mol·L-1],则需要加入Na2CO3固体的质量最少为________g。(保留小数点后1位有效数字)
(6)保持其他条件不变,在不同温度下对含镍废料进行酸浸,镍浸出率随时间变化如图。酸浸的最佳温度与时间分别为________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】自然界中的物质绝大多数以混合物的形式存在,为了便于研究和利用,常需对混合物进行分离和提纯。下列A、B、C、D是中学常见的混合物分离或提纯的装置。
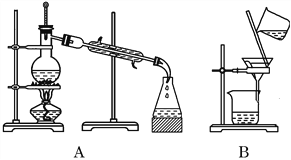
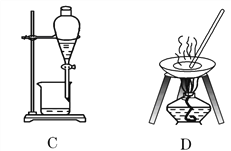
I.请根据混合物分离或提纯的原理,回答在下列实验中需要使用哪种装置。将A、B、C、D 填入适当的空格中。
(1)碳酸钙悬浊液中分离出碳酸钙______________________;
(2)氯化钠溶液中分离出氯化钠____________________;
(3)分离植物油和水____________________;
(4)分离酒精和水____________________;
(5)氯化钠溶液中分离出水____________________。
II.碘水中提取碘单质的方法如下:
(1)萃取分液
①下列可作为碘水中提取碘单质萃取剂的有__________
A.酒精 B.苯
②分液漏斗在使用前必须先________________;
③查资料得知:ρ(H2O)>ρ(苯)>ρ(酒精),若用①中所选萃取剂萃取碘水中的碘单质,分液时,水层应由分液漏斗的_______端口放出,有机层应由分液漏斗的________端口放出(此问填“上”或者“下”) ;
(2)蒸馏
①冷凝装置中冷凝水应该_______口进(填“上”或“下”)
②已知碘和四氯化碳的熔沸点数据如下表
熔点 | 沸点 | |
碘 | 113.7℃ | 184.3℃ |
四氯化碳 | -22.6℃ | 76.8℃ |
若用蒸馏法分离碘和四氯化碳的混合物,锥形瓶中先收集到的物质的名称是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】主族元素X、Y、Z、M、N的原子序数依次增大,X、Z和M分属于不同的周期,X、M元素可以形成负一价离子,Y原子的各能层电子数相同,Z原子最外层电子数是次外层的3倍,N元素原子的4p轨道上有3个未成对电子。
(1)五种元素中第一电离能最小的是________,电负性最大的是________。(填元素符号)
(2)Y元素原子的价层电子的电子排布图为________,该元素的名称是________。气态分子YM2的立体构型为________,YM2可形成多聚体(YM2)n的原因是________________。
(3)Z和N形成分子W的结构如图所示,化合物W的分子式为________,Z、N原子的杂化类型分别为________、________。

(4)已知化合物NX3是剧毒的气体,与AgNO3溶液反应有黑色Ag析出,同时生成W,此反应是检验微量NX3的方法,该反应的化学方程式是________________________________________________________________________。
(5)画出配离子YZ4X![]() 的结构式:________,1 mol该离子中含有的共价键数目为__________。
的结构式:________,1 mol该离子中含有的共价键数目为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】红葡萄酒密封储存时间越长,质量越好,原因之一是储存过程中生成了有香味的酯.在实验室也可以用如下图所示的装置制取乙酸乙酯,请回答下列问题.
(1)该实验反应物与生成物有机物的官能团种类有(填写名称).
(2)试管a中加入几块碎瓷片的目的是 .
(3)试管a中发生反应的化学方程式为 , 反应类型是 .
(4)反应开始前,试管b中盛放的溶液是 . 作用是 .
(5)反应结束后,振荡试管b,静置.反应结束后,试管b内的液体分成两层,乙酸乙酯在层(填写“上”或“下”).若分离10mL该液体混合物需要用到的主要玻璃仪器是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com