
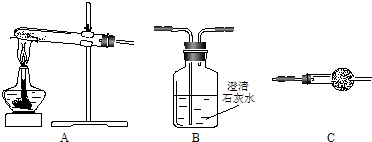
 £Ø2010?½š»ŖÄ£Äā£©ŅŃÖŖBa£ØAlO2£©2æÉČÜÓŚĖ®£®ČēÓŅĻĀĶ¼ŹĒĻņ100mL 0.02mol?L-1KAl£ØSO4£©2ČÜŅŗÖŠÖšµĪ¼ÓČė0.05mol?L-1Ba£ØOH£©2ČÜŅŗŹ±£Ø25”ę£©£¬Éś³É³ĮµķµÄĪļÖŹµÄĮæÓė¼ÓČėBa£ØOH£©2ČÜŅŗµÄĢå»żµÄ¹ŲĻµ£®ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©
£Ø2010?½š»ŖÄ£Äā£©ŅŃÖŖBa£ØAlO2£©2æÉČÜÓŚĖ®£®ČēÓŅĻĀĶ¼ŹĒĻņ100mL 0.02mol?L-1KAl£ØSO4£©2ČÜŅŗÖŠÖšµĪ¼ÓČė0.05mol?L-1Ba£ØOH£©2ČÜŅŗŹ±£Ø25”ę£©£¬Éś³É³ĮµķµÄĪļÖŹµÄĮæÓė¼ÓČėBa£ØOH£©2ČÜŅŗµÄĢå»żµÄ¹ŲĻµ£®ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©

 µć¾¦ŠĀ½Ģ²ÄČ«Äܽā¶ĮĻµĮŠ“š°ø
µć¾¦ŠĀ½Ģ²ÄČ«Äܽā¶ĮĻµĮŠ“š°ø Š”ѧ½Ģ²ÄĶźČ«½ā¶ĮĻµĮŠ“š°ø
Š”ѧ½Ģ²ÄĶźČ«½ā¶ĮĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
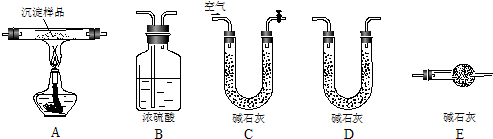
 £Ø2010?½š»ŖÄ£Äā£©°×Ž¼Ā«“¼¹ć·ŗ“ęŌŚÓŚŹ³Īļ£ØĄżČēɣ驔¢»ØÉś”¢ÓČĘäŹĒĘĻĢŃ£©ÖŠ£¬ĖüæÉÄܾßÓŠæ¹°©ŠŌ£®Äܹ»øś1Ħ¶ūøĆ»ÆŗĻĪļĘš·“Ó¦µÄBr2»ņH2µÄ×ī“óÓĆĮæ·Ö±šŹĒ£Ø””””£©
£Ø2010?½š»ŖÄ£Äā£©°×Ž¼Ā«“¼¹ć·ŗ“ęŌŚÓŚŹ³Īļ£ØĄżČēɣ驔¢»ØÉś”¢ÓČĘäŹĒĘĻĢŃ£©ÖŠ£¬ĖüæÉÄܾßÓŠæ¹°©ŠŌ£®Äܹ»øś1Ħ¶ūøĆ»ÆŗĻĪļĘš·“Ó¦µÄBr2»ņH2µÄ×ī“óÓĆĮæ·Ö±šŹĒ£Ø””””£©²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā
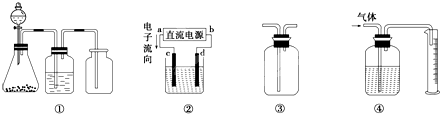
| 49n |
| 9m |
| 49n |
| 9m |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com