
 黄曲霉毒素M1是一种具有强致癌性的有机物,其分子结构如图所示.下列有关黄曲霉毒素M1的说法正确的是( )
黄曲霉毒素M1是一种具有强致癌性的有机物,其分子结构如图所示.下列有关黄曲霉毒素M1的说法正确的是( )| A. | 黄曲霉毒素M1的分子式为C17H14O7 | |
| B. | 黄曲霉毒素M1含有羟基,此羟基能被催化氧化为醛基 | |
| C. | 1mol黄曲霉毒素M1与NaOH溶液发生反应最多能消耗2molNaOH | |
| D. | 1mol黄曲霉毒素M1最多能与7molH2发生加成反应 |
分析 A.根据结构简式确定分子式;
B.该分子中含有醚键、醇羟基、碳碳双键、羰基和酯基,具有醚、醇、烯烃、酮和酯的性质;
C.黄曲霉毒素M1含有酯基,酯基水解后得到1个酚羟基;
D.苯环和碳碳双键、羰基能与氢气发生加成反应.
解答 解:A.由有机物结构可确定有机物分子式为C17H12O7,故A错误;
B.与羟基相连的C上无H,此羟基不能被氧化,故B错误;
C.黄曲霉毒素M1含有酯基,酯基水解后得到1个酚羟基,故1 mol黄曲霉毒素M1与NaOH溶液发生反应最多能消耗2 mol NaOH,故C正确;
D.黄曲霉素中,能与氢气发生加成反应的有1个苯环、2个碳碳双键和1个羰基,则1mol黄曲霉素可以和6molH2发生加成反应,故D错误,
故选C.
点评 本题考查有机物结构和性质,为高频考点,侧重考查醚、醇、烯烃、酮、酯的性质,明确官能团及其性质关系是解本题关键,易错选项是C,注意含有苯环.


科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤⑥⑦⑧ | B. | ①④⑥⑦⑧ | C. | ①⑧ | D. | ①④⑤⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 凡是有单质生成的分解反应一定是氧化还原反应 | |
| B. | CO与Fe2O3高温下反应为氧化还原反应,是置换反应 | |
| C. | 天然气的燃烧,不属于置换反应,为非氧化还原反应 | |
| D. | 1828年德国化学家维勒最先完成有机物的制取:NH4CNO$\frac{\underline{\;\;△\;\;}}{\;}$CO(NH2)2,该反应不属于四种反应类型中的任何一种,但属于氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 在化学反应中,${\;}_{1}^{1}$H2O可转变为D2O | |
| B. | “加碘食盐”生产中碘添加剂为单质I2 | |
| C. | 实验室用带玻璃塞的棕色瓶贮存液Br2 | |
| D. | 电解饱和MgCl2溶液时在阴极得到Mg |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
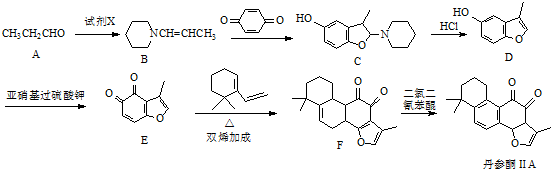
 .
. .
. 的合成路线流程图(无机试剂可任选).合成路线流程图示例如下:CH3CHO$→_{催化剂,△}^{O_{2}}$CH3COOH$→_{浓H_{2}SO_{4},△}^{CH_{3}CH_{2}OH}$CH3COOCH2CH3.
的合成路线流程图(无机试剂可任选).合成路线流程图示例如下:CH3CHO$→_{催化剂,△}^{O_{2}}$CH3COOH$→_{浓H_{2}SO_{4},△}^{CH_{3}CH_{2}OH}$CH3COOCH2CH3.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 若t1=15 s,用A的浓度变化表示t0~t1阶段的平均反应速率为0.004 mol•L-1•s-1 | |
| B. | t4~t5阶段改变的条件一定为减小压强 | |
| C. | 该容器的容积为2 L,B的起始物质的量为0.02 mol | |
| D. | t5~t6阶段,容器内A的物质的量减少了0.06 mol,而此过程中容器与外界的热交换总量为a kJ,该反应的热化学方程式3A(g)?B(g)+2C(g)△H=-50a kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 温度/℃ | 1000 | 1100 |
| 平衡常数 | 0.68 | 0.50 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加大量水稀释 | B. | 降低温度 | C. | 加少量NaOH | D. | 加少量CH3COONa |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com