
在恒温恒容的密闭容器中,能表明可逆反应X(g)+2Y(g)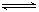 2Z(g)达到化学平衡状态的是
2Z(g)达到化学平衡状态的是
①X、Y、Z的物质的量之比为l∶2∶2 ②X、Y、Z的浓度不再发生变化
③容器中的压强不再发生变化 ④生成n mol Z的同时生成2n mol Y
A.①② B. ①④ C. ②③ D.③④
 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:
X、Y、Z、Q、M为常见的短周期元素,其原子序数依次增大。有关信息如下表:
| X | 动植物生长不可缺少的元素,是蛋白质的重要成分 |
| Y | 地壳中含量居第一位 |
| Z | 短周期中其原子半径最大 |
| Q | 生活中大量使用其合金制品,工业上可用电解其氧化物的方法制备 |
| M | 海水中大量富集的元素之一,其最高正价与负价的代数和为6 |
(1)X的气态氢化物的大量生产曾经解决了地球上因粮食不足而导致的饥饿和死亡问题,请写出该气态氢化物的电子式:____。
(2)已知37Rb和53I都位于第五周期,分别与Z和M位于同一主族、下列有关说法正确的是________________(填序号)。
A.原子半径:Rb>I
B.RbM中含有共价键
C.气态氢化物热稳定性:M >I
D.Rb、Q、M的最高价氧化物对应的水化物可以两两发生反应
(3)X、Y组成的一种无色气体遇空气变为红棕色。将标准状况下40 L该无色气体与15 L氧气通入一定浓度的NaOH溶液中,恰好被完全吸收,同时生成两种盐。请写出该反应的离子方程式________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
 对于反应2X(g)+Y(g)
对于反应2X(g)+Y(g)  2Z(g)在不同温度(T1和T2)及压强(p1和p2)下产物Z的物质的量n(Z)和反应时间t的关系如图所示,下列判断正确的是
2Z(g)在不同温度(T1和T2)及压强(p1和p2)下产物Z的物质的量n(Z)和反应时间t的关系如图所示,下列判断正确的是
A.T1<T2,p1<p2,正反应为放热反应
B.T1<T2,p1>p2,正反应为吸热反应
C.T1>T2,p1>p2,正反应为放热反应
D.T1>T2,p1<p2,正反应为吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应既属于氧化还原反应,又是吸热反应的是
A.锌粒与稀硫酸反应 B.灼热的木炭与CO2反应
C.铝粉与氧化铁粉末反应 D.Ba(OH)2·8H2O晶体与NH4Cl晶体反应
查看答案和解析>>
科目:高中化学 来源: 题型:
将甲烷与氯气按体积比1:1混合于一试管中并倒置于水槽里,置于光亮处,如图所示。下列叙述中,不正确的是
A.瓶中气体的黄绿色逐渐变浅 B.瓶内壁有油状液滴形成
C.此反应的生成物只有一氯甲烷 D.试管中液面上升

查看答案和解析>>
科目:高中化学 来源: 题型:
已知A、B、C、D、E是短周期的五种元素,它们的原子序数依次增大。通常A元素原子形成的离子核外电子数为零;C、D、E三种元素的最高价氧化物对应水化物之间可以两两反应;A与C同主族;B与E同主族;E的单质为黄色晶体,易溶于二硫化碳。
(1)写出B元素的名称: 。
(2)A与C能形成离子化合物CA,试画出其中阴离子的结构示意图 ;
(3)A、B、C三种元素形成的化合物所含的化学键类型为 。
(4)B、D、E三种元素的离子半径由大到小的顺序为 (用离子符号表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
元素周期表中某区域的一些元素多用于制造半导体材料,它们是
A.碱土金属元素
B.元素周期表中第3~12列的过渡元素
C.金属元素和非金属元素分界线附近的元素
D.左下方区域的金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
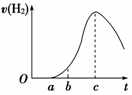
把在空气中久置的铝片5.0 g投入盛有500 mL 0.5 mol·L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间的关系可用如图曲线来表示。
请回答下列问题:
(1)曲线由O →a段不产生氢气的原因是 ,
 有关反应的化学方程式为______________________________________________;
有关反应的化学方程式为______________________________________________;
(2)曲线b→c段,产生氢气的速率增加较快的主要原因是
________________________________________________________________;
(3)曲线由c以后,产生氢气的速率逐渐下降的主要原因是
_________________________;
(4)该反应若使用催化剂,可使H2产量增多吗?______(填“会”或“不会”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
用铝粉和氧化铁粉末配成的铝热剂,分成两等份:一份在高温下恰好完全反应,再与足量稀硫酸反应,生成氢气aL;另一份直接放入足量烧碱溶液中充分反应,在相同条件下生气氢气bL,则体积比a:b为
A.1:1 B.3:2 C.2:3 D.1:4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com