
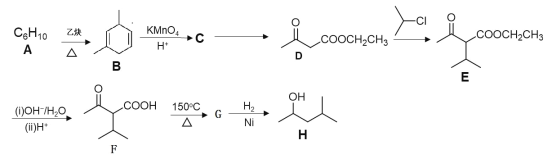
【题目】有机物H是优良的溶剂,在工业上可用作洗涤剂、润滑剂,其合成线路:
已知:①![]()
②![]()
③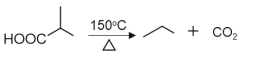
请回答下列问题:
(1)H的名称为___。用*标出F中的手性碳原子__(碳原子上连有4个不同原子或基团时,该碳称为手性碳)
(2)A的结构简式为___。
(3)D→E的化学方程式为___。
(4)F中含有官能团的名称为__。G→H的反应类型为__。
(5)写出符合下列条件的D的同分异构体的结构简式为__。
①能与NaHCO3溶液反应放出CO2②能发生银镜反应③核磁共振氢谱有4组峰且峰面积之比为6∶2∶1∶1
(6)请设计由![]() 和乙烯(CH2=CH2)为起始原料,制备
和乙烯(CH2=CH2)为起始原料,制备![]() 的合成路线__(无机试剂任选)。
的合成路线__(无机试剂任选)。
【答案】4—甲基—2—戊醇 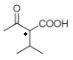
![]()
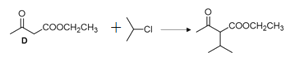 +HCl 羧基和羰基 加成反应(或还原反应)
+HCl 羧基和羰基 加成反应(或还原反应) 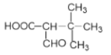 (或
(或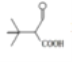 )
) 
【解析】
由题给有机物的转化关系可知,A和乙炔发生信息①反应生成B,则A的结构为![]() ; B与酸性高锰酸钾溶液发生信息②反应生成C,则C的结构为CH3COCH2COOH;C与乙醇在浓硫酸作用下共热反应生成D,D与
; B与酸性高锰酸钾溶液发生信息②反应生成C,则C的结构为CH3COCH2COOH;C与乙醇在浓硫酸作用下共热反应生成D,D与![]() 发生取代反应生成E,E发生水解反应生成F,F发生信息③反应生成G(
发生取代反应生成E,E发生水解反应生成F,F发生信息③反应生成G(![]() ),G与氢气发生加成反应生成H。
),G与氢气发生加成反应生成H。
(1)H的结构简式为![]() ,名称为4-甲基-2-戊醇;F的结构简式为
,名称为4-甲基-2-戊醇;F的结构简式为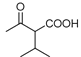 ,手性碳原子为连有4个不同原子或基团的饱和碳原子,F分子中与羧基相连的碳原子为连有4个不同原子或基团的手性碳原子,用*标出的结构简式为
,手性碳原子为连有4个不同原子或基团的饱和碳原子,F分子中与羧基相连的碳原子为连有4个不同原子或基团的手性碳原子,用*标出的结构简式为 ,故答案为:4-甲基-2-戊醇;
,故答案为:4-甲基-2-戊醇; ;
;
(2)由分析可知A的结构简式为![]() ,故答案为:
,故答案为:![]() ;
;
(3)D→E的反应为![]() 与
与![]() 发生取代反应生成
发生取代反应生成 ,反应的化学方程式为
,反应的化学方程式为![]() ,故答案为:
,故答案为:![]() ;
;
(4)F的结构简式为 ,含有官能团的名称为羧基和羰基;G→H的反应为在Ni做催化剂作用下,
,含有官能团的名称为羧基和羰基;G→H的反应为在Ni做催化剂作用下,![]() 与氢气加成反应生成
与氢气加成反应生成![]() ,故答案为:羧基和羰基;加成反应;
,故答案为:羧基和羰基;加成反应;
(5)D的结构简式为![]() ,D的同分异构体能与NaHCO3溶液反应放出CO2说明含有羧基,能发生银镜反应说明含有醛基,核磁共振氢谱有4组峰且峰面积之比为9∶1∶1∶1说明同一个碳原子上连有3个甲基,符合条件的同分异构体的结构简式可能为
,D的同分异构体能与NaHCO3溶液反应放出CO2说明含有羧基,能发生银镜反应说明含有醛基,核磁共振氢谱有4组峰且峰面积之比为9∶1∶1∶1说明同一个碳原子上连有3个甲基,符合条件的同分异构体的结构简式可能为 ,故答案为:
,故答案为: (或
(或 );
);
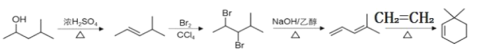
(6)结合题给信息可知,由![]() 和乙烯为起始原料制备
和乙烯为起始原料制备![]() 的步骤为
的步骤为![]() 在浓硫酸作用下发生下去反应得到
在浓硫酸作用下发生下去反应得到![]() ,
,![]() 与溴发生加成反应得到
与溴发生加成反应得到![]() ,
,![]() 在氢氧化钠乙醇作用下发生消去反应
在氢氧化钠乙醇作用下发生消去反应![]() ,
,![]() 和乙烯发生加成反应得到
和乙烯发生加成反应得到![]() ,合成路线为
,合成路线为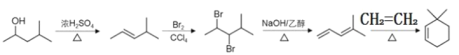 ,故答案为:
,故答案为: 。
。


 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案科目:高中化学 来源: 题型:
【题目】450℃时,在某恒容密闭容器中存在反应:C(s)+2NO(g)![]() N2(g)+CO2(g),下列说法能作 为判断该反应达到化学平衡状态标志的是
N2(g)+CO2(g),下列说法能作 为判断该反应达到化学平衡状态标志的是
A. 容器内压强保持不变B. v正(N2)=2v逆(NO)
C. N2与CO2的物质的量之比为1∶1D. 容器内混合气体的密度保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中进行A(g)+2B(s)![]() 2C(s)+3D(s) ΔH>0的反应,下列说法正确的是( )
2C(s)+3D(s) ΔH>0的反应,下列说法正确的是( )
A. 升高温度,正反应速率增大,逆反应速率减小
B. 容器内气体平均相对分子质量不变时达到化学平衡状态
C. 温度不变,增大B的投入量,正反应速率增大
D. 温度不变,压缩容器体积重新达到平衡后,A的浓度不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家提出由 WO3 催化乙烯和 2-丁烯合成丙烯的反应历程如图(所有碳原子满足最外层八电子结构)。下列说法不正确的是
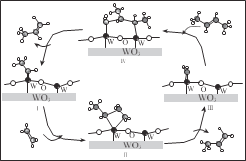
A.乙烯、丙烯和 2-丁烯互为同系物
B.乙烯、丙烯和 2-丁烯的沸点依次升高
C.Ⅲ→Ⅳ中加入的 2-丁烯具有反式结构
D.碳、钨(W)原子间的化学键在Ⅲ→Ⅳ→Ⅰ的过程中未发生断裂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2能使酸性KMnO4溶液褪色,反应为2KMnO4+5SO2+2H2O=2MnSO4+K2SO4+2H2SO4
(1)用双线桥(或单线桥)标出下列反应中电子转移的方向和数目。___
2KMnO4+5SO2+2H2O=2MnSO4+K2SO4+2H2SO4
(2)该反应中还原剂是___,还原产物是___。
(3)若有1molKMnO4完全反应,则转移的电子的物质的量是___mol,参加反应的SO2气体标准状况下体积为___L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在燃烧2.24L(标准状况)CO与O2的混合气体时,放出11.32kJ的热量,最后产物的密度为原来气体密度的1.25倍,则CO的燃烧热为
A. 283 kJ·mol-1 B. -283 kJ·mol-1 C. -566 kJ·mol-1 D. 566kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用一定浓度的盐酸溶液滴定某氨水溶液。滴定终点附近溶液pH和导电能力的变化分别如下图所示(利用溶液导电能力的变化可判断滴定终点,溶液总体积变化忽略不计)。下列说法错误的是
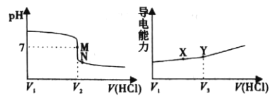
A.M点对应溶液中c(NH4+)=c(Cl-)
B.X→Y溶液导电性增强的主要原因是c(H+)和c(Cl-)增大
C.根据溶液pH和导电能力的变化可判断V2<V3
D.M→N过程中 不变
不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关NaHCO3和Na2CO3的性质,以下叙述错误的是
A.等质量的NaHCO3和Na2CO3与足量盐酸反应,在相同条件下Na2CO3产生的CO2体积小
B.等物质的量的两种盐与同浓度盐酸完全反应,所消耗盐酸的体积Na2CO3是NaHCO3的两倍
C.等质量NaHCO3和Na2CO3与盐酸完全反应,前者消耗盐酸较多
D.等物质的量的NaHCO3和Na2CO3与足量盐酸反应产生CO2一样多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】饮用水的质量关系到关系到每个人的健康,因含有一定浓度的NO3-将对人类健康产生危害,NO3-能氧化人体血红蛋白中的Fe(II),使其失去携氧功能,为了降低饮用水中NO3-的浓度,某兴趣小组提出如图方案:
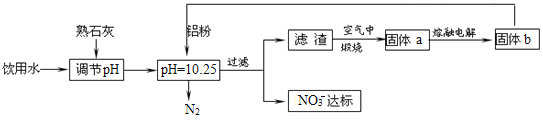
请回答下列问题:
(1)人体血液中如果缺乏亚铁离子,就会造成缺铁性贫血。市场出售的某种麦片中含有微量、颗粒细小的还原铁粉,这些铁粉在人体胃酸(胃酸的主要成分是HCl)作用下转化成亚铁盐。写出该反应的离子方程式:____。
(2)已知过滤后得到的滤渣是一种混合物,则在溶液中铝粉和NO3-反应的离子方程式为__。
(3)该方案中选用熟石灰调节pH,理由是___、___。
(4)用H2催化还原法也可降低饮用水中NO3-的浓度,已知反应中的还原产物和氧化产物均可参与大气循环,则催化还原法的离子方程式为___。
(5)饮用水中的NO3-主要来自于NH4+。已知在微生物作用的条件下,NH4+经过两步反应被氧化成NO3-。两步反应的能量变化示意图如图,试写出1molNH4+(aq)全部氧化成NO3-(aq)的热化学方程式是____。
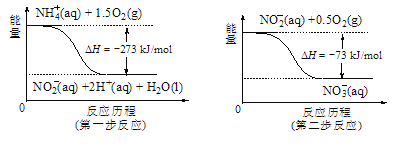
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com