
| 碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 | |
| A | 纯碱 | 硫酸 | 小苏打 | 氧化钙 | 干冰 |
| B | 烧碱 | 盐酸 | 食盐 | 氧化钠 | 一氧化碳 |
| C | 石灰水 | NaHSO4 | 碳酸钙 | 过氧化钠 | 二氧化碳 |
| D | NH3•H2O | HNO3 | 明矾 | 氧化铁 | SO3 |
| A. | A | B. | B | C. | C | D. | D |
分析 碱指电离时产生的阴离子全部都是氢氧根离子的化合物;
酸指电离时产生的阳离子全部都是氢离子的化合物;
盐指电离时生成金属阳离子(或NH4+)和酸根离子的化合物;
碱性氧化物指与水反应生成碱的氧化物或能跟酸起反应生成一种盐和水的氧化物(且生成物只能有盐和水,不可以有任何其它物质生成);
酸性氧化物是指能与水作用生成酸或与碱作用生成盐和水的氧化物(且生成物只能有一种盐和水,不可以有任何其它物质生成).
解答 解:A.纯碱是碳酸钠,是由钠离子和碳酸根离子构成的盐不是碱,故A错误;
B.盐酸是氯化氢水溶液,为混合物,酸为纯净物;一氧化碳是不成盐氧化物,不属于酸性氧化物,故B错误;
C.石灰水是氢氧化钙与水的混合物,碱为纯净物,NaHSO4是盐不是酸,Na2O2与酸反应除了生成盐和水,还生成氧气,不属于碱性氧化物,故C错误;
D.NH3•H2O是弱碱,HNO3是酸,明矾是盐,氧化铁是碱性氧化物,三氧化硫与水化合为硫酸,与氢氧化钠反应生成硫酸钠和水,属于酸性氧化物,故D正确;
故选D.
点评 本题是对物质的化学式及分类的考查,对物质的名称、分类及化学式有较明确的认识即可顺利解答,属基础知识考查题,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | Na 和O2 | B. | NaOH 和 CO2 | C. | AlCl3 和氨水 | D. | Na2CO3 和HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 23:24:27 | B. | 1:2:3 | C. | 6:3:2 | D. | 6:2:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
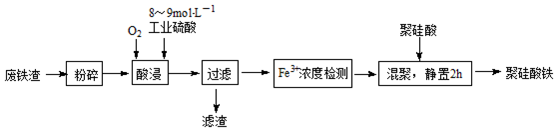

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该物质可能是金属钠 | B. | 该物质一定是钠的化合物 | ||
| C. | 该物质一定含钠元素 | D. | 该物质中可能含钾元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用湿润的pH试纸测稀碱液的pH,测定值偏大 | |
| B. | NaCl溶液和CH3COONH4溶液均显中性且两溶液中水的电离程度相同 | |
| C. | 用pH试纸测定次氯酸钠溶液的pH | |
| D. | 除去工业废水中的Cu2+可以选用FeS作沉淀剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

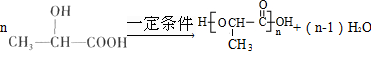 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
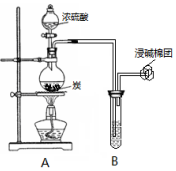 某小组同学利用如图装置开展实验,请回答:
某小组同学利用如图装置开展实验,请回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com