
| A、氢氧化铜与盐酸反应:H++OH-═H2O |
| B、金属钠与水反应:2Na+2H2O═2Na++2OH-+H2↑ |
| C、盐酸与硝酸银溶液反应:Ag++Cl-═AgCl↓ |
| D、碳酸钙溶于稀盐酸:CaCO3+2H+═Ca2++CO2↑+H2O |


科目:高中化学 来源: 题型:
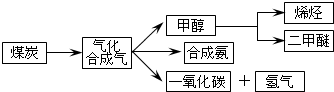
| c(H2)?c(CO) |
| c(H2O) |
| 物质 | CH3OH | CH3OCH3 | H2O |
| c(mol/L) | 0.8 | 1.24 | 1.24 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向冰醋酸中加水至配成醋酸稀溶液的过程H+的浓度逐渐减小 |
| B、实验室制氢气,为了加快反应速率,可向稀H2SO4中滴加少量Cu(NO3)2溶液 |
| C、常温时,pH=2的CH3COOH溶液和HCl溶液、pH=12的氨水和NaOH溶液,四种溶液中由水电离的c(H+)相等 |
| D、常温下,将稀NaOH溶液与CH3COOH溶液混合,可能出现pH>7,且c(OH-)>c(Na+)>c(H+)>c(CH3COO-)的情况 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、构成原电池正极和负极的材料必须是两种金属 |
| B、由铜、锌作电极与硫酸铜溶液组成的原电池中铜是负极 |
| C、马口铁(镀锡铁)破损时与电解质溶液接触,锡先被腐蚀 |
| D、镁.铝作电极,与硫酸构成原电池,电流由铝经导线流向镁 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、仅①②③④ | B、仅②③④⑤ |
| C、仅①②④⑥ | D、都有可能 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、能使酚酞变红的溶液:Na+、Ba2+、NO3-、Cl- |
| B、含有0.1mol?L-1 Fe3+的溶液中:K+、Mg2+、I-、SO42- |
| C、能溶解Al(OH)3的溶液:NH4+、K+、SO42-、HCO3- |
| D、c(Al3+)=0.5mol?L-1的溶液中:Na+、K+、[Al(OH)4]-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、汽车尾气的排放是雾霾形成的重要原因之一 |
| B、运载火箭升空的动力主要来自化学能 |
| C、“玉兔”月球车太阳能电池帆板的材料是二氧化硅 |
| D、玻璃纤维是玻璃钢的增强体,其组成属于无机非金属材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 W、X、Y、Z是四种常见的短周期主族元素,其原子半径随原子序数的变化如图所示.已知Y、Z两种元素的单质是空气的主要成分,W原子的最外层电子数与Ne原子的最外层电子数相差1.下列说法正确的是( )
W、X、Y、Z是四种常见的短周期主族元素,其原子半径随原子序数的变化如图所示.已知Y、Z两种元素的单质是空气的主要成分,W原子的最外层电子数与Ne原子的最外层电子数相差1.下列说法正确的是( )| A、Y、W的最简单氢化物的水溶液都呈酸性 |
| B、X、Y与Z中的任意两种元素均可形成两种或两种以上的化合物 |
| C、上述四种元素形成的化合物都抑制水的电离 |
| D、W的单质可从Z的最简单氢化物中置换出Z的单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||||
B、n=
| ||||
C、m/65<n=
| ||||
D、
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com