
【题目】按要求填空。
(1)氢能是发展中的新能源,它的利用包括氢的制备、储存和应用三个环节。回答下列问题:
①与汽油相比,氢气作为燃料的优点是_____________________(至少答出两点)。
②利用太阳能直接分解水制氢,是最具吸引力的制氢途径,其能量转化形式为____________。
(2)有机物M经过太阳光光照可转化成N,转化过程如下:
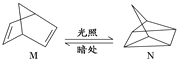 ΔH=+88.6 kJ·mol-1。则M、N相比,较稳定的是____________。
ΔH=+88.6 kJ·mol-1。则M、N相比,较稳定的是____________。
(3)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛一定比例混合高温下煅烧,产物可作耐高温材料,4Al(s)+3TiO2(s)+3C(s)===2Al2O3(s)+3TiC(s)ΔH=-1 176 kJ·mol-1,则反应过程中,每转移1 mol电子放出的热量为______________。
(4)在一定温度下,4 L密闭容器内某一反应中气体M、气体N的物质的量随时间变化的曲线如图:
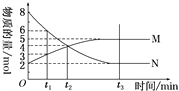
①该反应的化学方程式为____________________________。
②若t2=2 min,计算反应开始至t2时刻用M的浓度变化表示的平均反应速率为______________。
③t2时刻,反应物的转化率为______________。
【答案】 污染小;可再生;来源广;资源丰富;燃烧热值高(任写其中2个) 光能转化为化学能 M 98 kJ 2N![]() M 0.25 mol·L-1·min-1 75%
M 0.25 mol·L-1·min-1 75%
【解析】(1)①与汽油相比,氢气作为燃料的优点有污染小、可再生、来源广、资源丰富、燃烧热值高等,故答案为:污染小、可再生、来源广、资源丰富、燃烧热值高等;
②利用太阳能直接分解水制氢,是将光能转化为化学能,故答案为:将光能转化为化学能;
(2)有机物M经过太阳光光照可转化成N的△H=+88.6kJmol-1,过程是吸热反应,N暗处转化为M,是放热反应,能量越低越稳定,说明M稳定,故答案为:M;
(3)由反应可知,转移12mol电子放出1176kJ热量,则每转移1mol电子放出的热量为![]() =98kJ,故答案为:98kJ;
=98kJ,故答案为:98kJ;
(4)①由图象可以看出,反应中N的物质的量减小,M的物质的量增多,则N为反应物,M为生成物,且△n(N):△n(M)=6mol:3mol=2:1,则反应的化学方程式为:2N![]() M,故答案为:2N
M,故答案为:2N![]() M;
M;
②根据v=![]() 计算得M的平均化学反应速率为
计算得M的平均化学反应速率为 =0.25mol/(Lmin),故答案为:0.25mol/(Lmin);
=0.25mol/(Lmin),故答案为:0.25mol/(Lmin);
③根据图像可知,从反应开始N的物质的量在减小,所以N为反应物,N的转化率为![]() ×100%=75%,故答案为:75%。
×100%=75%,故答案为:75%。


 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:
【题目】分子式为C8H10O的芳香族化合物,遇三氯化铁溶液不显色,能与金属钠反应放出氢气,满足条件的同分异构体有( )
A.大于10种
B.10种
C.6种
D.5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知: C(s)+O2(g)═CO2(g)△H1
CO2(g)+C(s)═2CO(g)△H2
2CO(g)+O2(g)═2CO2(g)△H3
4Fe(s)+3O2(g)═2Fe2O3(s)△H4
3CO(g)+Fe2O3(s)═3CO2(g)+2Fe(s)△H5
下列关于上述反应焓变的判断正确的是( )
A.△H1>0,△H3<0
B.△H2>0,△H4>0
C.△H1=△H2+△H3
D.△H3=△H4+△H5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【选修5:有机化学基础】具有抗菌作用的白头翁素衍生物H的合成路线如图所示

已知: ①.RCH2Br ![]() R﹣HC═CH﹣R′
R﹣HC═CH﹣R′
②.R﹣HC═CH﹣R′![]()
![]()
③.R﹣HC═CH﹣R′![]()

(以上R、R'、R'代表氢、烷基或芳基等)
(1)A属于芳香烃,其名称是____。C中官能团的名称是____。
(2)H的分子式为____,由G生成H的反应类型为____。
(3)试剂a的结构简式是____,试剂b为____。
(4)由C生成D的化学方程式是____。
(5)E与I2在一定条件下反应生成F的产物不唯一,此反应同时生成另外一种有机副产物且与F互为同分异构体,此有机副产物的结构简式是____。
(6)下列说法正确的是____。
A.E中含有3种官能团
B.1mol H与足量NaOH溶液反应,消耗2mol NaOH
C.由F生成G的反应是消去反应
D.1mol G最多可以与3mol H2发生加成反应
(7)与化合物C具有相同官能团且属于芳香族化合物的同分异构体共有____种(包括C本身)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随原子序数的递增,八种短周期元素(用字母X表示)原子半径的相对大小、最高正价或最低负价的变化如图所示. 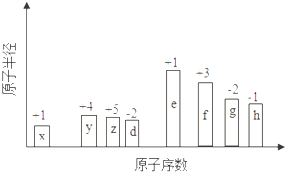
根据判断出的元素回答问题:
(1)y的元素名称 , 它位于元素周期表中第周期第族.
(2)h的最高价氧化物的化学式为 .
(3)d、g两种元素的最简单氢化物中稳定性比较强的物质,其结构式是 .
(4)x、z两元素可形成含有10个电子的分子,该分子的电子式为 . 位于第四周期且与z同主族的元素,其气态氢化物的化学式为 .
(5)e、f 两种元素最高价氧化物对应的水化物发生反应的离子方程式为 .
(6)将1mol e的单质在足量d 2中燃烧,所得产物中含有阴离子的数目为 , 含有的化学键为 . a.离子键 b.极性共价键 c.非极性共价键
(7)由x、d两种元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号) . a.MnO2 b.FeCl3 c.Na2SO3 d.K2SO4 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com