
一定温度下,反应N2(g)+3H2(g) 2NH3(g)达到化学平衡状态的标志是( )
2NH3(g)达到化学平衡状态的标志是( )
A.N2、H2和NH3的物质的量分数不再改变
B.c(N2)∶c(H2)∶c(NH3)=1∶3∶2
C.N2与H2的物质的量之和是NH3的物质的量的2倍
D.单位时间里每增加1 mol N2,同时增加3 mol H2
科目:高中化学 来源: 题型:
下列反应过程中,同时有离子键、极性共价键和非极性共价键的断裂和形成的反应是 ( )
A.NH4Cl NH3↑+HCl↑
NH3↑+HCl↑
B.NH3+CO2+H2O NH4HCO3
NH4HCO3
C.2NaOH+Cl2 NaCl+NaClO+H2O
NaCl+NaClO+H2O
D.2Na2O2+2CO2 2Na2CO3+O2
2Na2CO3+O2
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)已知反应A+3B 2C+D,在30 s内A的浓度减小了0.5 mol·L-1,则此段时间内以B的浓度变化表示的反应速率为
2C+D,在30 s内A的浓度减小了0.5 mol·L-1,则此段时间内以B的浓度变化表示的反应速率为
mol·L-1·min-1,以C的浓度变化表示的反应速率为 mol·L-1·min-1。
(2)在恒温恒容条件下,反应2SO2+O2 2SO3进行一段时间后,SO3的浓度增加了0.4 mol·L-1,在这段时间内用O2表示的反应速率为0.04 mol·L-1·s-1,则这段时间为 s。
2SO3进行一段时间后,SO3的浓度增加了0.4 mol·L-1,在这段时间内用O2表示的反应速率为0.04 mol·L-1·s-1,则这段时间为 s。
(3)将物质的量相等的A、B混合于2 L密闭容器中,发生如下反应:3A(g)+B(g)
 xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol·L-1,c(A)∶c(B)=3∶5,
xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol·L-1,c(A)∶c(B)=3∶5,
C的平均反应速率是0.1 mol·L-1·min-1。回答下列问题:
①x值是 。
②用B表示的5 min内的平均反应速率为_______________________________。
③反应开始前放入容器中的A、B物质的量各为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是实验室干馏煤的装置图,回答下列问题:
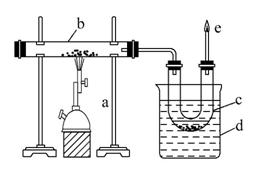
(1)指出图中仪器名称:
c ,d 。
(2)仪器d的作用是 ,
c中液体有 和 ,其中无机物里溶有 ,可用 检验出来。有机物可以通过 的方法使其中的重要成分分离出来。
(3)e处点燃的气体主要成分有 ,
火焰的颜色 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下图为氢氧燃料电池原理示意图,按照此图的提示,下列叙述不正确的是
( )
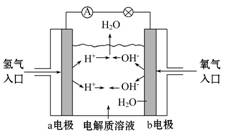
A.b电极是正极
B.总反应方程式为2H2+O2====2H2O
C.负极发生还原反应,正极发生氧化反应
D.氢氧燃料电池是一种具有广泛应用前景的绿色电源
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)在25℃时,向100 mL含氯化氢14.6 g的盐酸溶液里放入5.60 g纯铁粉(不考虑反应前后溶液体积的变化),反应开始至
2 min末,收集到1.12 L(标准状况)氢气。在此之后,又经过4 min,铁粉完全溶解。则前2 min与后4 min相比,反应速率较快的是 ,其原因是 。
(2)在1×105Pa和25℃时,H—H键、N≡N键和N—H键的键能分别为436 kJ·mol-1、945 kJ·mol-1和391 kJ·mol-1,
①根据上述数据判断工业合成氨的反应是 (填“吸热”或“放热”)反应;
②在25℃时,取1 mol氮气和3 mol氢气放入一密闭容器中,在催化剂存在下进行反应。理论上放出或吸收的热量为Q1,则Q1为 kJ;
③实际生产中,放出或吸收的热量为Q2,Q1与Q2比较,正确的是 。
A.Q1>Q2 B.Q1<Q2 C.Q1=Q2
如此选择的理由是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
将NH4HCO3在试管中加热,使放出的气体依次通过盛有足量Na2O2的干燥管、足量浓H2SO4的洗气瓶(假设每步反应气体完全反应),最后得到的气体是( )
A.NH3 B.O2
C.H2O D.CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是四种盐的溶解度(g)。
|
| 0 | 10 | 20 | 30 | 40 | 60 | 80 | 100 |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.3 | 38.4 | 39.8 |
| NaNO3 | 73 | 80 | 88 | 96 | 104 | 124 | 148 | 180 |
| KCl | 27.6 | 31 | 34.0 | 37.0 | 40.0 | 45.5 | 51.1 | 56.7 |
| KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 110.0 | 169 | 246 |
请设计一个从硝酸钠和氯化钾制备纯硝酸钾晶体的实验(要求写出化学方程式及实验步骤)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com