
【题目】元素周期表是学习化学的重要工具,它隐含着许多信息和规律。请根据下表中短周期元素的原子半径和主要化合价,回答表后问题。
① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
原子半径(10-10 m) | 0.74 | 1.60 | 0.53 | 1.10 | 0.99 | 1.11 | 0.75 | 1.43 |
最高或最低化合价 | +2 | +1 | +5 | +7 | +2 | +5 | +3 | |
-2 | -3 | -1 | -3 |
(1)元素①在周期表中的位置为_____。
(2)元素①、⑦的氢化物的稳定性由强到弱的顺序为____(填化学式)。
(3)元素①、③形成的18电子化合物的电子式为____,元素②、⑧的最高价氧化物对应的水化物中,碱性较强的是______(填化学式)。
(4)元素②、⑤形成化合物的电子式为_____。
(5)元素⑤的最高价氧化物对应的水化物的水溶液与元素⑧的最高价氧化物对应水化物反应的离子方程式为
【答案】第二周期 VIA H2O>NH3 H2O2电子式![]() Mg(OH)2 MgCl2电子式
Mg(OH)2 MgCl2电子式![]() 3H+ + Al(OH)3 = Al3+ + 3H2O
3H+ + Al(OH)3 = Al3+ + 3H2O
【解析】
原子的电子层数越多,其原子半径越大,同一周期元素中,原子半径随着原子序数的增大而减小,同一主族中,原子半径随着原子序数的增大而增大,根据化合价和原子半径可以判断⑥为铍、②为Mg,①的原子半径小于铍且其最低负价是-2,元素的最低负价=其最外层电子数-8,所以①位于第VIA族,为O元素,③的原子半径小于铍且其最高正价为+1,故为氢,⑦的原子半径小于铍且其最低负价是-3,元素的最低负价=其最外层电子数-8,所以⑦位于第VA族,是氮元素,这几种元素都是短周期元素,其余为第三周期元素,结合其主要化合价知,④是P元素、⑤是Cl元素、⑧是Al元素,结合元素周期律、原子结构来分析。
(1)元素①位于第VIA族,为O元素,在周期表中的位置为第二周期 VIA。
(2)非金属性越强,氢化物越稳定,O的非金属性大于N,则氢化物的稳定性由强到弱的顺序为H2O>NH3。
(3)元素①、③形成的18电子化合物为H2O2,电子式为![]() ;元素②为Mg、⑧是Al,Mg金属性强,最高价氧化物对应的水化物中,碱性较强的是Mg(OH)2。
;元素②为Mg、⑧是Al,Mg金属性强,最高价氧化物对应的水化物中,碱性较强的是Mg(OH)2。
(4)元素②、⑤形成的常见化合物是MgCl2,氯化镁为离子化合物,其电子式为![]() 。
。
(5)元素⑤的最高价氧化物对应的水化物的水溶液是高氯酸,与元素⑧的最高价氧化物对应水化物氢氧化铝反应的离子方程式为3H++ Al(OH)3═Al3++3H2O。


 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案科目:高中化学 来源: 题型:
【题目】如图是一种利用锂电池“固定CO2”的电化学装置,在催化剂的作用下,该电化学装置放电时可将CO2转化为C和Li2CO3,充电时选用合适催化剂,仅使Li2CO3发生氧化反应释放出CO2和02。下列说法中正确的是

A. 该电池充电时,阳极反应式为:C+2Li2CO3-4e-=3CO2↑+4Li
B. 该电池放电时,Li+向电极X方向移动
C. 该电池充电时,电极Y与外接直流电源的负极相连
D. 该电池放电时,每转移4mol电子,理论上生成1molC
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在图(Ⅰ)所示的装置中,烧杯中盛放的是Ba(OH)2溶液,当从滴定管中逐渐加入某种溶液A时,溶液的导电性的变化趋势如图(Ⅱ)所示。
(Ⅰ)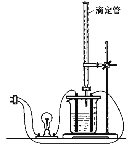 (Ⅱ)
(Ⅱ)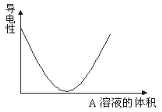
(1)滴加液体至图(Ⅱ)中曲线最低点时,灯泡可能熄灭,可能的原因是______________。
(2)试根据离子反应的特点分析,溶液A中含有的溶质可能是(填序号)____________。
①HCl ②H2SO4 ③NaHSO4 ④NaHCO3
(3)已知0.1 mol·L-1NaHSO4溶液中c(H+)=0.1 mol·L-1,请回答下列问题:
①写出NaHSO4在水溶液中的电离方程式_______________________________。
②NaHSO4属于________(填“酸”、“碱”或“盐”)。
③向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至中性,请写出发生反应的离子方程式:_______;在以上中性溶液中,继续滴加Ba(OH)2溶液,请写出此步反应的离子方程式:_________。写出NaHSO4溶液与NaHCO3溶液混合的离子方程式_________。
(4)有以下物质:①石墨; ②氯化氢气体; ③酒精; ④铝; ⑤二氧化碳; ⑥碳酸氢钠固体;⑦氢氧化钡溶液; ⑧液态醋酸; ⑨氯化银固体; ⑩氨气。
①其中能导电的是:____________________________;
②属于非电解质的是:__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香豆素是广泛存在于植物中的一类芳香化合物,大多具有光敏性,有的还具有抗菌和消炎作用。它的核心结构是芳香内酯A,其分子式为C9H6O2,该芳香内酯A经下列步骤转变为水杨酸和和化合物E。
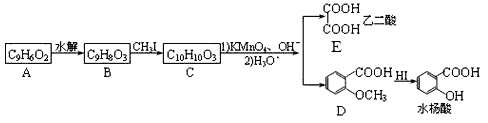
已知:CH3CH = CHCH2CH3![]() CH3COOH + CH3CH2COOH
CH3COOH + CH3CH2COOH
请回答下列问题:
(1)C中官能团的名称为________;化合物A的结构简式为________。
(2)C生成D和E的反应类型为________,化合物E的化学名称是________。
(3)写出B→C的化学反应方程式_________ 。
(4)化合物D有多种同分异构体,其中一类同分异构体是苯的二元取代物,且水解后生成的产物之一能发生银镜反应。这类同分异构体共有________种;写出其中核磁共振氢谱有4种峰,且其信号强度之比为1:2:2:3的一种同分异构体的结构简式________ 。
(5)已知: R- CH=CH2![]() R-CH2CH2Br,请设计合理方案由
R-CH2CH2Br,请设计合理方案由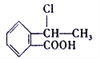 合成
合成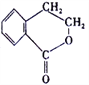 (其他无机原料自选,用反应流程图表示,并注明反应条件)。_______。示例:原料
(其他无机原料自选,用反应流程图表示,并注明反应条件)。_______。示例:原料![]() ……产物
……产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将足量的CO2不断通入NaOH、Ba(OH)2、NaAlO2的混合溶液中〔已知NaAlO2与CO2反应生成Al(OH)3〕,则生成沉淀的物质的量与通入CO2的体积的关系可表示为( )
A.  B.
B. 
C.  D.
D. 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶波中加入铝粉能产生氢气,则该溶液中不可能大量共存的一组离子是
A. K+、Cl-、H+ B. NH4+、NO3-、SO42- C. K+、A13+、Br- D. Na+、K+、SiO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若N60与C60结构相似的另一种“足球分子”,则下列说法正确的是
A. N60分子中只含有共价键 B. N60和14N都是氮的同位素
C. N60是一种新型化合物 D. N60与C60互为同素异形体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把铁片放入盛有过量稀硫酸的试管中,不影响氢气产生速率的因素是( )
A. 硫酸的浓度B. 铁片的表面积
C. 溶液的温度D. 加少量Na2SO4固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,分别向10 mL 0.1 molL1的NaOH 溶液中逐滴加入0.1 molL1的一元酸HA和HB溶液,用pH传感器测得混合溶液的pH变化曲线如图所示,下列说法正确的是
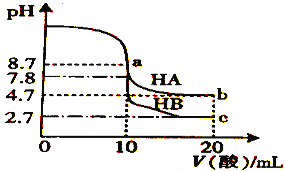
A. HA的酸性强于HB的酸性
B. V(酸)=10mL时,两份溶液中c(B)=c(A)
C. a 点时,c(A)>c(Na+)>c(OH)>c(H+)
D. b、c点时,c(A)+c(HA)=2c(Na+)=c(HB)+c(B)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com