
| A. | 1-丁烯 | B. | 二甲苯 | C. | 苯 | D. | 环己烷 |
分析 A.1-丁烯的分子式为C4H8,含有32个电子,12个原子;
B.二甲苯的分子式为C8H10,含有8×6+10×1=58个电子,18个原子;
C.苯的分子式为C6H6,含有6×6+6=42个电子,12个原子,一定条件下,苯能发生加成反应和取代反应;
D.环己烷不能发生加成反应.
解答 解:A.1-丁烯的分子式为C4H8,含有32个电子,12个原子,电子总数比原子个数多20个,故A错误;
B.二甲苯的分子式为C8H10,含有8×6+10×1=58个电子,18个原子,电子总数比原子个数多40个,故B错误;
C.苯的分子式为C6H6,含有6×6+6=42个电子,12个原子,电子总数比原子个数多30个,一定条件下,苯能发生加成反应和取代反应,故C正确;
D.环己烷不能发生加成反应,故D错误;
故选C.
点评 本题考查了常见有机物的结构和化学性质,难度不大,做题时可先根据能发生化学反应的类型判断,再计算电子数和原子数进行排除.


科目:高中化学 来源: 题型:选择题
| A. | MgCl2和H2O | B. | Mg(OH)2、HCl和H2O | C. | Mg、Cl2和H2O | D. | MgO、HCl和H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
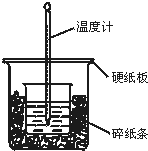 50mL 0.50mol•L-1盐酸与50mL 0.55mol•L-1NaOH溶液在图示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
50mL 0.50mol•L-1盐酸与50mL 0.55mol•L-1NaOH溶液在图示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 任何晶体中,若含有阳离子也一定含有阴离子 | |
| B. | 原子晶体中只含有共价键 | |
| C. | 离子晶体中只含有离子键 | |
| D. | 分子晶体中只存在分子间作用力,不含化学键 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 和双酚A:
和双酚A: 缩聚而成,其反应方程式为
缩聚而成,其反应方程式为 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C6H12N4 | B. | C4H8N4 | C. | C6H10N4 | D. | C6H8N2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH${\;}_{4}^{+}$+D2O?NH3•D2O+H+ | B. | NH${\;}_{4}^{+}$+D2O?NH3•HDO+D+ | ||
| C. | c(OD-)•c(H+)=Kw | D. | c(OH-)•c(D+)=Kw |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com