(2012?吉林一模)为测定FeO和Fe
2O
3固体混合物中Fe元素的含量,可用氢气还原一定质量的此混合物并测定生成水的质量的方法来完成.若在实验室中选用下列实验装置来实现上述目的(图中夹持装置已略去,部分装置可重复使用).请填空:
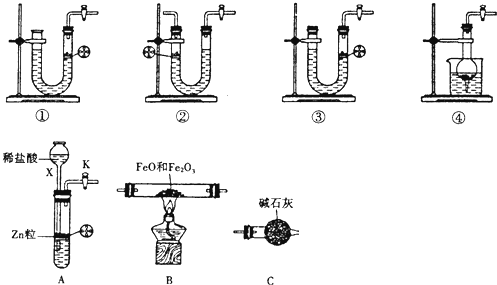
(1)仪器X的名称是
长颈漏斗
长颈漏斗
.
(2)装置A中发生反应的离子方程式为
Zn+2H+=Zn2++H2↑
Zn+2H+=Zn2++H2↑
,实验前检验装置A的气密性的方法是
关闭活塞K,向长颈漏斗中加水至其液面高于试管中的液面,(停止加水)一段时间后液面高度差没变化,说明装置不漏气
关闭活塞K,向长颈漏斗中加水至其液面高于试管中的液面,(停止加水)一段时间后液面高度差没变化,说明装置不漏气
.
(3)装置B中发生反应的化学方程式为
FeO+H
2Fe+H
2O或Fe
2O
3+3H
22Fe+3H
2O
FeO+H
2Fe+H
2O或Fe
2O
3+3H
22Fe+3H
2O
(任写一个即可).
(4)图①-④示装置中与A装置具有相同作用的是
①④
①④
(填装置编号).
(5)按正确的实验设计,所连接的装置顺序为:A→C→
B
B
→
C
C
→
C
C
.
(6)若FeO和Fe
2O
3混合物的质量为ag,反应完全后生成水的质量为bg,则混合物中Fe元素的质量分数为
(用含字母的数学式表示).



