
【题目】下列反应的离子方程式书写不正确的是( )
A.硫酸与Na2SiO3溶液混合:SiO![]() +2H+===H2SiO3↓
+2H+===H2SiO3↓
B.Cl2和NaOH溶液反应:Cl2+2OH-===Cl-+ClO-+H2O
C.向亚硫酸氢钠溶液中滴加硫酸氢钠溶液:H++HSO![]() ===SO2↑+H2O
===SO2↑+H2O
D.向硫酸铵溶液中加入氢氧化钡溶液:Ba2++SO![]() ===BaSO4↓
===BaSO4↓
【答案】D
【解析】
A.硫酸与Na2SiO3溶液生成硫酸钠和硅酸,硫酸是强酸,硅酸钠、硫酸钠均为可溶性盐,三者均为强电解质,离子方程式书写中均能改写成离子,故离子方程式为:SiO![]() +2H+=H2SiO3↓,A正确;
+2H+=H2SiO3↓,A正确;
B.Cl2和NaOH溶液反应生成氯化钠、次氯酸钠和水,故离子方程式为:Cl2+2OH-=Cl-+ClO-+H2O,B正确;
C.由于亚硫酸是中强酸,故亚硫酸氢钠在水溶液中电离出Na+和HSO![]() ,而硫酸是强酸,故硫酸氢钠溶液在水溶液中电离出Na+、H+和SO
,而硫酸是强酸,故硫酸氢钠溶液在水溶液中电离出Na+、H+和SO![]() ,故该反应的离子方程式为:H++HSO
,故该反应的离子方程式为:H++HSO![]() =SO2↑+H2O,C正确;
=SO2↑+H2O,C正确;
D.向硫酸铵溶液中加入氢氧化钡溶液,由于硫酸铵电离出的![]() 和氢氧化钡电离出的OH-也会反应生成氨气和水,故该反应的离子方程式为:2
和氢氧化钡电离出的OH-也会反应生成氨气和水,故该反应的离子方程式为:2![]() +Ba2++SO
+Ba2++SO![]() +2OH-=BaSO4↓+2NH3↑+2H2O,D错误;
+2OH-=BaSO4↓+2NH3↑+2H2O,D错误;
故答案为:D。


 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案科目:高中化学 来源: 题型:
【题目】莽草酸可用于合成药物达菲,其结构简式如图,下列关于莽草酸的说法正确的是
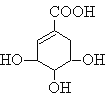
A.分子式为C7H6O5
B.分子中含有2种官能团
C.可发生加成和取代反应
D.在水溶液羧基和羟基均能电离出H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,对可逆反应4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g),下列叙述中错误的是( )
4NO(g)+6H2O(g),下列叙述中错误的是( )
A.生成NO的速率与消耗NO的速率相等,反应达到平衡状态
B.当O2物质的量浓度不再变化时,反应达到平衡状态
C.达到化学平衡时,若升高温度,则正反应速率增大,逆反应速率也增大
D.单位时间内生成x mol NO,同时消耗x mol NH3,反应达平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视。目前工业上有一种方法是用CO2生产燃料甲醇:在容器为1L的密闭容器中充入1molCO2和3molH2 ,平衡时CO2的物质的量为0.25mol,CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)。该反应进行过程中能量的变化(单位为kJ·mol-1)如图所示。
CH3OH(g)+H2O(g)。该反应进行过程中能量的变化(单位为kJ·mol-1)如图所示。

请回答下列问题:
(1)观察图象可知上述反应过程中,断裂反应物中的化学键吸收的总能量______(填“大于”“小于”或“等于”)形成生成物中的化学键释放的总能量。
(2)甲醇的结构类似于乙醇,试写出甲醇的结构式:__________。甲醇分子中的化学键类型是________(填“离子键”或“共价键”)。
(3)科研人员开发出一种新型甲醇燃料电池。其电解质溶液是KOH溶液,在该电池的负极发生反应的物质是__________,发生的是__________(填"氧化"或"还原")反应。
(4)欲使合成甲醇的化学反应速率加快,请写出两条措施:___________________
(5)平衡时H2的转化率为__________平衡时混合气体中CH3OH(g)的体积分数为__________。
(6)下列事实能表明该反应已达平衡状态的是(_______)(填序号)
A.CO2(g)的浓度不再发生变化
B.单位时间内消耗1mol CO2的同时生成3mol H2
C.在一个绝热的容器中,混合物的温度不再发生变化
D.在一个容积固定的容器内,压强不再发生变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨硼烷(NH3·BH3)电池可在常温下工作,装置如图所示。未加入氨硼烷之前,两极室质量相等,电池反应为NH3·BH3+3H2O2=NH4BO2+4H2O。已知两极室中电解质足量,下列说法正确的是( )
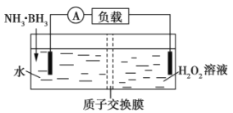
A.正极的电极反应式为2H++2e-═H2↑
B.电池工作时,H+通过质子交换膜向负极移动
C.电池工作时,正、负极分别放出H2和NH3
D.工作一段时间后,若左右两极室质量差为1.9g,则电路中转移0.6mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在金属Pt、Cu和铱(Ir)的催化作用下,密闭容器中的H2可高效转化酸性溶液中的硝态氮(NO3)以达到消除污染的目的。其工作原理的示意图如下:
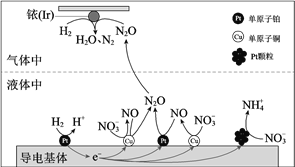
下列说法不正确的是
A. Ir的表面发生反应:H2 + N2O == N2 + H2O
B. 导电基体上的负极反应:H2-2e == 2H+
C. 若导电基体上只有单原子铜,也能消除含氮污染物
D. 若导电基体上的Pt颗粒增多,不利于降低溶液中的含氮量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的量相同的铜片分别与体积相同且过量的浓硝酸、稀硝酸反应,下列有关二者的比较相等的是( )
①反应中氧化剂得到的电子总数 ②铜片消耗完所需时间
③反应后溶液中的铜离子浓度(反应前后溶液体积不变) ④反应生成气体的体积(同温、同压)
A.①③B.②④C.①④D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,向10mL0.1mol·L-1一元弱碱XOH溶液中逐滴滴加0.1mol·L-1的HCl溶液,溶液的AG[AG=lg![]() ]变化如图所示(溶液混合时体积变化忽略不计)。下列说法正确的是
]变化如图所示(溶液混合时体积变化忽略不计)。下列说法正确的是
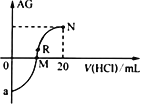
A.若a=-8,则25℃时,0.1mol·L-1XOH溶液的pH=8
B.M点表示盐酸和XOH恰好完全反应
C.R点溶液中可能存在c(X+)+c(XOH)=c(Cl-)
D.M点到N点,水的电离程度逐渐减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 18g氨基(-ND2)中含有的电子数为10NA
B. 一定质量的乙烷与22.4L(标准状况)Cl2在光照条件下发生取代反应,形成C-Cl键的数目为2NA
C. 用惰性电极电解100mL0.1mol·L-1的CuSO4溶液,当阴、阳两极产生相同条件下等体积的气体时,电路中转移电子数为0.04NA
D. n(H2SO3)和n(HSO3-)之和为1mol的KHSO3溶液中,含有的K+数目为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com