
| A、原子半径 X>Y>Z |
| B、非金属性X>Y>Z |
| C、阴离子的还原性 X->Y2->Z3- |
| D、气态氢化物的稳定性 HX<H2Y<ZH3 |


 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案科目:高中化学 来源: 题型:
| A、异丁烷 | B、乙烷 | C、丙烷 | D、丁烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、4L0.5 mol?L-1NaCl溶液 |
| B、1L0.3 mol?L-1的Na2SO4溶液 |
| C、0.8L0.4 mol?L-1NaOH溶液 |
| D、2L0.15 mol?L-1Na3PO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 陈述Ⅰ | 陈述Ⅱ用作呼吸面具的供氧剂 |
| A | Si原子最外层有4个电子 | 单质及其氧化物硬度很大 |
| B | SO2具有漂白性 | SO2可使溴水褪色 |
| C | Na2O2能与CO2、H2O反应 | Na2O2 |
| D | 钠比铜活泼 | 钠可以与硫酸铜溶液反应置换出铜 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
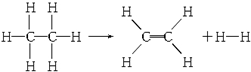
| A、该反应放出251.2 kJ的热量 |
| B、该反应吸收251.2 kJ的热量 |
| C、该反应放出125.6 kJ的热量 |
| D、该反应吸收125.6 kJ的热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2O2晶体中阴离子和阳离子 | ||
| B、NaHSO4晶体中阳离子和阴离子 | ||
C、
| ||
| D、氯化钠中的质子总数和电子总数 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SO2、O2 |
| B、SO2、SO3 |
| C、O2、SO3 |
| D、SO2、O2、SO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com