
【题目】下列溶液中有关物质的浓度关系正确的是( )
A.c(NH ![]() )相等的(NH4)2SO4、NH4HSO4、NH4Cl溶液:c(NH4HSO4)>c[(NH4)2SO4]>c(NH4Cl)
)相等的(NH4)2SO4、NH4HSO4、NH4Cl溶液:c(NH4HSO4)>c[(NH4)2SO4]>c(NH4Cl)
B.等物质的量的NaClO、NaHCO3混合溶液:c(HClO)+c(ClO﹣)=c(HCO ![]() )+c(H2CO3)+c(CO
)+c(H2CO3)+c(CO ![]() )
)
C.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO﹣)>c(H+)>c(OH﹣)
D.某二元弱酸的酸式盐NaHA溶液中:c(H+)+c(Na+)=c(OH﹣)+c(HA﹣)+c(A2﹣)
【答案】B
【解析】解:A、NH4HSO4电离出的氢离子抑制铵根离子水解,c(NH4+)相等的(NH4)2SO4、NH4HSO4、NH4Cl溶液中,c[(NH4)2SO4]<c(NH4HSO4)<c(NH4Cl),故A错误;B、根据物料守恒,碳与氯元素在溶液中存在的所有微粒浓度相等,所以c(HClO)+c(ClO﹣)=c(HCO ![]() )+c(H2CO3)+c(CO
)+c(H2CO3)+c(CO ![]() ),故B正确;
),故B正确;
C、向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液呈酸性,c(Na+)<c(CH3COO﹣),故C错误;
D、在二元弱酸的酸式盐NaHA溶液中,根据电荷守恒可以c(H+)+c(Na+)=c(OH﹣)+c(HA﹣)+2c(A2﹣),故D错误;
故选B.


科目:高中化学 来源: 题型:
【题目】DAP﹣A树脂是一种优良的热固性树脂,被用作高级UV油墨的一种成分.这种材料可采用如下合成路线制备: 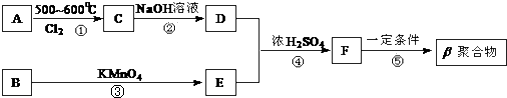 已知:
已知:
Ⅰ. ![]()
![]()
![]()
Ⅱ.β聚合物的结构简式: 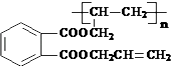
试回答下列问题:
(1)在①~④的反应中属取代反应的是 .
(2)写出反应②的化学方程式 .
(3)写出反应⑤的化学方程式
(4)工业上可由C经过两步反应制得甘油,这两步反应的反应类型依次是和 .
(5)写出B(C8H10)苯环上的所有二氯代物结构简式: , 其中核磁共振氢谱只有两组峰,且峰面积比为3:1的有种.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常用含少量SiO2、Al2O3的铬铁矿(FeO·Cr2O3)冶炼铬,简要流程如下:
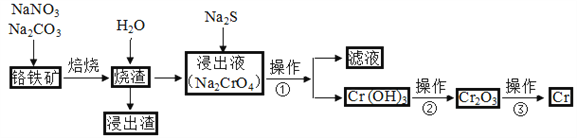
(1)完成下列化学方程式(在横线上填写物质的化学式及计量数):
2FeO·Cr2O3+4Na2CO3+7NaNO3![]() 4Na2CrO4+Fe2O3+4CO2↑+________。
4Na2CrO4+Fe2O3+4CO2↑+________。
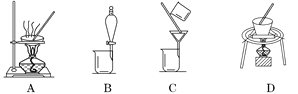
(2)操作①包括过滤与洗涤,在实验室中进行洗涤沉淀的操作是_____________________;操作②可选用的装置(部分夹持装置略去)是________(填序号)。
(3)写出能够完成操作③的相关反应的化学方程式:__________________________________。
(4)化学需氧量(COD)可度量水遭受有机物污染的程度。在强酸并加热的条件下,用K2Cr2O7作强氧化剂处理水样,并测定消耗的K2Cr2O7的量,然后换算成相当于O2的含量称为化学需氧量(以mg·L-1计)。化学兴趣小组测定某水样的化学需氧量(COD)过程如下:
a.取a mL水样置于锥形瓶中,加入10.00 mL 0.2500 mol·L-1的K2Cr2O7溶液。
b.……
c.加指示剂,用c mol·L-1的硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液滴定,终点时消耗b mL(此步骤的目的是用Fe2+把多余的Cr2O![]() 转化为Cr3+)。
转化为Cr3+)。
①计算该水样的化学需氧量时需用到下列关系:要除去1 mol Cr2O![]() 需消耗_______ mol Fe2+,1 mol Cr2O
需消耗_______ mol Fe2+,1 mol Cr2O![]() 相当于________mol O2。
相当于________mol O2。
②该废水中加入硫酸亚铁铵和稀硫酸,发生反应的离子方程式为______________________。
③若用硫酸亚铁铵[(NH4)2Fe(SO4)2]处理该含铬(Cr2O![]() )废水过程中,反应中铁元素和铬元素完全转化为沉淀。该沉淀经干燥后得到nmolFeO·FeyCrxO3。不考虑处理过程中的实际损耗,下列叙述正确的是____。
)废水过程中,反应中铁元素和铬元素完全转化为沉淀。该沉淀经干燥后得到nmolFeO·FeyCrxO3。不考虑处理过程中的实际损耗,下列叙述正确的是____。
a.消耗硫酸亚铁铵的物质的量为1.5nmol
b.处理废水中的Cr2O72-的物质的量为0.25nmol
c.反应中发生转移的电子数为3nxmol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1摩尔气态烃A最多和2摩尔HCl加成,生成氯代烷B,1摩尔B与4摩尔Cl2发生取代反应,生成只含碳、氯两种元素的C.则A的分子式为( )
A.C2H2
B.C2H4
C.C3H4
D.C4H6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,把试管放入盛有25℃的饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5mL盐酸于试管中。试回答下列回答:

(1)实验中观察到的现象是_______________。(选填代号)
A.试管中镁片逐渐溶解 B.试管中产生无色气泡
C.烧杯外壁变冷 D.烧杯底部析出少量白色固体
(2)试管中发生的反应属于_____________(选填“氧化还原反应”或“非氧化还原反应”)。
(3)写出有关反应的离子方程式________________。
(4)由实验推知,MgCl2溶液和H2的总能量______(填“大于”“小于”“等于”)镁片和盐酸的总能量。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】资源化利用二氧化碳不仅可减少温室气体的排放,还可重新获得燃料或重要工业产品.
(1)有科学家提出可利用FeO吸收和利用CO2 , 相关热化学方程式如下:6FeO(s)+CO2(g)=2Fe3O4(s)+C(s)△H=﹣76.0kJmol﹣1
①上述反应中每生成1mol Fe3O4 , 转移电子的物质的量为mol.
②已知:C(s)+2H2O(g)=CO2 (g)+2H2(g)△H=+113.4kJmol﹣1 , 则反应:
3FeO(s)+H2O (g)=Fe3O4 (s)+H2 (g)的△H= .
(2)在一定条件下,二氧化碳转化为甲烷的反应如下:CO2(g)+4H2 (g)CH4 (g)+2H2O(g)△H=QkJmol﹣1 , 向一容积为 2L的恒容密闭容器中充人2molCO2和8mol H2 , 在 300℃时发生上述反应,达到平衡时,测得CH4的浓度为0.8molL﹣1 , 则300℃时上述反应的平衡常数K= . 200℃时该反应的平衡常数K=64.8,则该反应的Q(填“>”或“<”)0.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是元素周期表的一部分,①~⑨是元素周期表中的部分元素。
ⅠA | 0 | |||||||
① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
…… | ② | ③ | ④ | |||||
⑤ | ⑥ | …… | ⑦ | ⑧ | ⑨ | |||
请回答下列问题:
(1)⑥的元素符号是_______ ,⑦的离子结构示意图 _______________________,原子半径⑤______⑥(填“>”或“<”)。
(2)元素②③④的气态氢化物中最稳定的是______________(填化学式)。
(3)元素⑤的最高价氧化物对应的水化物与元素⑨的氢化物的水溶液发生反应的离子方程式是_________________________________。
(4)元素①和②形成的化合物的电子式是_____________________。
(5)元素非金属性⑧_______⑨(填“>”或“<”)。
(6)已知元素⑧的原子序数为a,则元素③的原子序数可能为___________。
A、a + 8 B、a-8 C、a + 2 D、a-2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的量浓度相同的NaCl、MgCl2、AlCl3三种溶液,当溶液的体积比为3:2:1时,三种溶液中Cl-的物质的量浓度之比为( )
A. 1:1:1 B. 1:2:3 C. 3:2:1 D. 3:4:3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com