
 ).
).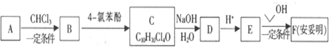
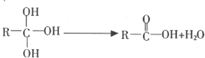 ;
;
 .
. 与O2反应的化学方程式2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
与O2反应的化学方程式2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.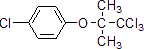 .
.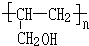 .
.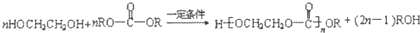
 生成中间体N,N与
生成中间体N,N与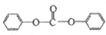 合成工程塑料M(
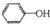
合成工程塑料M(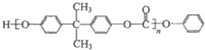 ),则由N合成M的聚合反应方程式为n
),则由N合成M的聚合反应方程式为n +n
+n $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$ +(2n-1)
+(2n-1) .
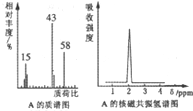
. 分析 由A的质谱图可知A的相对分子质量为58,5.8g有机物A的物质的量为0.1mol,燃烧生成CO2为$\frac{6.72L}{22.4L/mol}$=0.3mol,生成H2O为$\frac{5.4g}{18g/mol}$=0.3mol,则A分子中C原子数目为$\frac{0.3mol}{0.1mol}$=3、H原子数目为$\frac{0.3mol×2}{0.1mol}$=6,故含有O原子数目为$\frac{58-12×3-6}{16}$=1,则A的分子式为C3H6O,A的核磁共振氢谱只有1个吸收峰,则A的结构简式为 .E与乙醇反应生成安妥明,逆推可知E为
.E与乙醇反应生成安妥明,逆推可知E为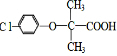 ,D为
,D为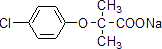 ,由C的分子式,又由羟基在一个碳上不稳定,结合信息②可知C为
,由C的分子式,又由羟基在一个碳上不稳定,结合信息②可知C为 ,则B为
,则B为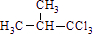 .
.
解答 解:由A的质谱图可知A的相对分子质量为58,5.8g有机物A的物质的量为0.1mol,燃烧生成CO2为$\frac{6.72L}{22.4L/mol}$=0.3mol,生成H2O为$\frac{5.4g}{18g/mol}$=0.3mol,则A分子中C原子数目为$\frac{0.3mol}{0.1mol}$=3、H原子数目为$\frac{0.3mol×2}{0.1mol}$=6,故含有O原子数目为$\frac{58-12×3-6}{16}$=1,则A的分子式为C3H6O,A的核磁共振氢谱只有1个吸收峰,则A的结构简式为 .E与乙醇反应生成安妥明,逆推可知E为
.E与乙醇反应生成安妥明,逆推可知E为 ,D为
,D为 ,由C的分子式,又由羟基在一个碳上不稳定,结合信息②可知C为
,由C的分子式,又由羟基在一个碳上不稳定,结合信息②可知C为 ,则B为
,则B为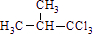 .
.
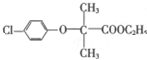
(1)降血脂药物F(安妥明)分子中含氧官能团的名称为酯基、醚键,E→F的反应类型是:酯化反应或取代反应,
故答案为:酯基、醚键;酯化反应或取代反应;
(2)4-氯苯酚(又名对氯苯酚)的结构简式是: ,
,
故答案为: ;
;
(3)Cu催化下条件下 与O2反应的化学方程式:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O,
与O2反应的化学方程式:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O,
故答案为:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O;
(4)C的结构简式是 ,
,
故答案为: ;
;
(5)A的结构简式为 ,A的一种同分异构体能与Na反应,还能发生加聚反应,该同分异构体为CH2=CHCH2OH,加聚产物的结构简式为
,A的一种同分异构体能与Na反应,还能发生加聚反应,该同分异构体为CH2=CHCH2OH,加聚产物的结构简式为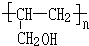 ,
,
故答案为: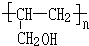 ;
;
(6)若将1molA( )与2mol
)与2mol 生成中间体N,N与
生成中间体N,N与 合成工程塑料M(
合成工程塑料M( ),可知N为
),可知N为 ,则由N合成M的聚合反应方程式为:n
,则由N合成M的聚合反应方程式为:n +n
+n $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$ +(2n-1)
+(2n-1) ,
,
故答案为:n +n
+n $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$ +(2n-1)
+(2n-1) .
.
点评 本题考查有机物的合成与推断,题目难度中等,注意根据题给信息确定A的分子式和结构,结合F的结构简式采用倒推法推断,对学生的逻辑推理有较高的要求.


科目:高中化学 来源: 题型:选择题
| 选项 | X | Y | Z | M |
| A | H2S | S | SO3 | O2 |
| B | Mg | C | CO | CO2 |
| C | NaOH | Na2CO3 | NaHCO3 | CO2 |
| D | NH3 | NO | NO2 | O2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向滴加有KSCN的FeCl2溶液,不断滴加氯水 | 溶液颜色先变红后褪色 | Fe2+先是被氧化为Fe3+,后来又被还原为Fe2+ |
| B | 向浓盐酸中加入少量碳酸钠溶液,将产生的气体通入苯酚钠溶液 | 苯酚钠溶液中出现白色浑浊 | 实验有缺陷,不能证明酸性:盐酸>碳酸>苯酚 |
| C | 在酸性KMnO4溶液中通入SO2 | 溶液褪色 | SO2具有漂白性 |
| D | 用标准浓度的烧碱溶液滴定未知浓度的盐酸,酚酞做指示剂 | 锥形瓶内溶液颜色由无色变为浅红色立即停止滴定 | 酸碱恰好中和 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
| 实验装置 |  | 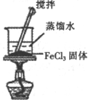 | 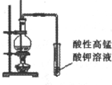 |  |
| 实验目的 | 比较非金属性强弱S>C>Si | 制取少量的Fe(OH)3胶体 | 证明乙醇与浓H2SO4共热生成了乙烯 | 比较不同催化剂的催化效果 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | M的分子式为C5H10O | |
| B. | 该中性有机物有4种(不考虑立体异构) | |
| C. | 上述过程发生的所有反应与油脂化反应的反应类型相同 | |
| D. | M和N都可以发生取代反应、都能与Na反应生成H2,因此具有相同官能团 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷和氯气光照条件下反应 | B. | CH3CH2CHBrCH3发生消去反应 | ||
| C. | 1,3-丁二烯与Br2发生加成反应 | D. | 乙烯和氯化氢发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | ||
| W | Z | ||
| T |
| A. | 气态氢化物的稳定性:Y>W>X | |
| B. | X、Y两种元素形成的化合物只有两种 | |
| C. | 物质WY2、W3X4、WZ4均有熔点高、硬度大的特性 | |
| D. | T元素的单质具有半导体的特性,T与Z元素可形成化合物TZ4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com