
| ŹµŃé²½Öč | ²Ł×÷ | ĻÖĻóÓė½įĀŪ |
| µŚŅ»²½ | ȔɣĮæŅŗĢå×°ÓŚŹŌ¹Ü£¬ĻņŹŌ¹ÜÖŠµĪČė¼øµĪKSCNČÜŅŗ | |
| µŚ¶ž²½ | ČōČÜŅŗ×ĻÉ«ĶŹČ„£¬ŌņĖµĆ÷ŗ¬ÓŠFe2+£¬ČōĪŽĆ÷ĻŌ±ä»Æ£¬ŌņĖµĆ÷²»ŗ¬Fe2+ |
·ÖĪö £Ø1£©ĻõĖįµÄĪļÖŹµÄĮæÅضČc=$\frac{n}{V}$=$\frac{\frac{m}{M}}{V}$=$\frac{\frac{m}{V}}{M}$=$\frac{¦Ń}{M}$¼ĘĖć£»
£Ø2£©øł¾ŻŅ»Ńõ»ÆµŖ¼«Ņ×ŗĶæÕĘųÖŠµÄO2·“Ó¦¼°ÓėæÕĘųĆÜ¶Č½Ó½ü½Ē¶ČÅŠ¶Ļ£»
£Ø3£©ĢśŗĶĻ”ĻõĖį·“Ӧɜ³ÉŅ»Ńõ»ÆµŖ£¬Ņ»Ńõ»ÆµŖ»įŃøĖŁ±»Ńõ»ÆĪŖ¶žŃõ»ÆµŖ£¬NO”¢¶žŃõ»ÆµŖ¶¼ÓŠ¶¾£¬ŠčŅŖĪüŹÕ“¦Ąķ£»
£Ø4£©¶žŃõ»ÆµŖŗĶĖ®·“Ó¦²śĪļŹĒŅ»Ńõ»ÆµŖ£»
£Ø5£©øł¾ŻŃõ»Æ»¹Ō·“Ó¦ÖŠµĆŹ§µē×ÓŹżÄæĻąµČĄ“»Ų“š£»
£Ø6£©ĢśŗĶĻõĖį·“Ó¦µÄ²śĪļČ”¾öÓŚĢśµÄĮæµÄ¶ąÉŁ£¬ŃĒĢśĄė×Ó¾ßÓŠ»¹ŌŠŌ£¬ÄÜŹ¹øßĆĢĖį¼ŲĶŹÉ«£¬Čż¼ŪĢśÓöKSCNČÜŅŗĻŌŗģÉ«£®
½ā“š ½ā£ŗ£Ø1£©ĻõĖįµÄĪļÖŹµÄĮæÅضČc=$\frac{n}{V}$=$\frac{\frac{m}{M}}{V}$=$\frac{\frac{m}{V}}{M}$=$\frac{¦Ń}{M}$=$\frac{1890g/L”Į5%}{63g/mol}$=1.5mol•L-1£¬¹Ź“š°øĪŖ£ŗ1.5mol•L-1£»
£Ø2£©Ņ»Ńõ»ÆµŖ¼«Ņ×ŗĶæÕĘųÖŠµÄO2·“Ó¦£¬ĒŅÓėæÕĘųĆÜ¶Č½Ó½ü£¬ĖłŅŌ²»ÄÜÓĆÅÅæÕĘų·Ø£¬¹Ź“š°øĪŖ£ŗNOÓėæÕĘųÖŠµÄO2·“Ó¦£¬NOÓėæÕĘųĆÜ¶Č½Ó½ü£»
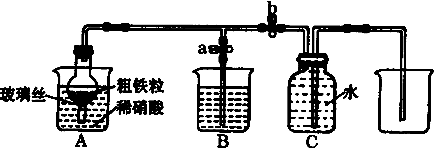
£Ø3£©ĢśŗĶĻ”ĻõĖį·“Ӧɜ³ÉŅ»Ńõ»ÆµŖ£¬Ņ»Ńõ»ÆµŖ»įŃøĖŁ±»Ńõ»ÆĪŖ¶žŃõ»ÆµŖ£¬ĖłŅŌA×°ÖƵÄøÉŌļ¹ÜÖŠ¹Ū²ģµ½µÄĻÖĻóŹĒ£ŗ½šŹō²»¶ĻČܽā£¬ÓŠĘųĢå²śÉśÖš½„±äĪŖŗģ×ŲÉ«£»µŖµÄŃõ»ÆĪļÓŠ¶¾£¬ŠčŅŖÓĆÉÕ¼īČÜŅŗĪüŹÕ£¬
¹Ź“š°øĪŖ£ŗ½šŹō²»¶ĻČܽā£¬ÓŠĘųĢå²śÉśÖš½„±äĪŖŗģ×ŲÉ«£»ĪüŹÕµŖµÄŃõ»ÆĪļ£»
£Ø4£©¶žŃõ»ÆµŖŗĶĖ®·“Ó¦²śĪļŹĒŅ»Ńõ»ÆµŖ£¬ĖłŅŌČōČ„µōB×°ÖĆ£¬¶ŌŹÕ¼ÆŅ»Ńõ»ÆµŖ²»»į²śÉśÓ°Ļģ£¬
¹Ź“š°øĪŖ£ŗĪŽÓ°Ļģ£»
£Ø5£©Ńõ»Æ»¹Ō·“Ó¦ÖŠµĆŹ§µē×ÓŹżÄæĻąµČ£¬FeŗĶHNO3¾łĪŽŹ£Óą£¬½šŹōĢśČ«×Ŗ»ÆĪŖŃĒĢś£¬ĢśŹ§µē×ÓµÄĮæĪŖ2amol£¬½šŹōĢśČ«×Ŗ»ÆĪŖČż¼ŪĢś£¬ĢśŹ§µē×ÓµÄĮæĪŖ3amol£¬½šŹōĢśµÄÉś³ÉĪļ¼ČÓŠŃĒĢśĄė×ÓÓÖÓŠČż¼ŪĢśĄė×ÓŹĒ£¬ĢśŹ§µē×ÓµÄĮæ¾Ķ2a”«3amolÖ®¼ä£¬ĻõĖįĻŌŹ¾ĖįŠŌŗĶŃõ»ÆŠŌ£¬ĻŌŹ¾ĖįŠŌµÄĻõĖįŗĶ±ķĻÖŃõ»ÆŠŌµÄĻõĖįµÄĪļÖŹµÄĮæÖ®±Č¾łĪŖ3£ŗ1£¬“ĖŹ±ĻõĖįµÄ×ŖŅʵē×ÓµÄĮæĪŖ£ŗ$\frac{3b}{4}$mol£¬
¹Ź“š°øĪŖ£ŗ$\frac{3b}{4}$mol£Ø2a mol»ņ3amol»ņ2amol”«3amol£©£»
£Ø6£©ĢśĻą¶ŌÓŚĻõĖį¹żĮæŹ±£¬²śĪļÖ»ÓŠŃĒĢśĄė×Ó£¬ŃĒĢśĄė×Ó¾ßÓŠ»¹ŌŠŌ£¬ÄÜŹ¹øßĆĢĖį¼ŲĶŹÉ«£¬ČōĢśĻą¶ŌÓŚĻõĖį²»×揱£¬²śĪļÖ»ÓŠČż¼ŪĢśĄė×Ó£¬Čż¼ŪĢśÓöKSCNČÜŅŗĻŌŗģÉ«£¬ÓŠæÉÄÜĢśµÄĮ½ÖÖ¼ŪĢ¬¾ł“ęŌŚ£¬¹Ź²Ł×÷·½·Ø¼°ĻÖĻóĪŖ£ŗ
| ŹµŃé²½Öč | ²Ł×÷ | ĻÖĻóÓė½įĀŪ |
| µŚŅ»²½ | ȔɣĮæŅŗĢå×°ÓŚŹŌ¹Ü£¬ĻņŹŌ¹ÜÖŠµĪČė¼øµĪKSCNČÜŅŗ | ČōČÜŅŗ±äŃŖŗģÉ«£¬ĖµĆ÷ŗ¬Fe3+£¬ČōČÜŅŗĪŽĆ÷ĻŌ±ä»Æ£¬ĖµĆ÷²»ŗ¬Fe3+ |
| µŚ¶ž²½ | ȔɣĮæŅŗĢå×°ÓŚŹŌ¹Ü£¬ĻņŹŌ¹ÜÖŠµĪČė¼øµĪĖįŠŌKMnO4ČÜŅŗ | ČōČÜŅŗ×ĻÉ«ĶĖČ„£¬ŌņĖµĆ÷ŗ¬ÓŠFe2+£¬ČōĪŽĆ÷ĻŌ±ä»Æ£¬ŌņĖµĆ÷²»ŗ¬Fe2+ |
| ŹµŃé²½Öč | ²Ł×÷ | ĻÖĻóÓė½įĀŪ |
| µŚŅ»²½ | ČōČÜŅŗ±äŃŖŗģÉ«£¬ĖµĆ÷ŗ¬Fe3+£¬ČōČÜŅŗĪŽĆ÷ĻŌ±ä»Æ£¬ĖµĆ÷²»ŗ¬Fe3+ | |
| µŚ¶ž²½ | ȔɣĮæŅŗĢå×°ÓŚŹŌ¹Ü£¬ĻņŹŌ¹ÜÖŠµĪČė¼øµĪĖįŠŌKMnO4ČÜŅŗ |
µćĘĄ ±¾Ģā±¾Ģāæ¼²éŠŌÖŹŹµŃé·½°øµÄÉč¼Ę£¬ĢāÄæÄѶČÖŠµČ£¬ŹŌĢā×ŪŗĻŠŌ½ĻĒ攢ÖŖŹ¶µć½Ļ¶ą£¬Éę¼°»Æѧ¼ĘĖć”¢ŹµŃé·½°øµÄÉč¼ĘÓėĘĄ¼Ū”¢³£¼ūĪļÖŹµÄŠŌÖŹ¼°¼ģŃé·½·ØµČÖŖŹ¶£¬ŠčŅŖѧɜ¾ßÓŠŌśŹµµÄ»ł“”ÓėŌĖÓĆÖŖŹ¶·ÖĪö½ā¾öĪŹĢāµÄÄÜĮ¦£¬×¢Ņā»ł“”ÖŖŹ¶µÄĄķ½āÕĘĪÕ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³£ĪĀĻĀ£¬10L pH=1µÄĮņĖįČÜŅŗÖŠŗ¬ÓŠµÄH+ŹżĪŖNA | |
| B£® | ½«58.5g NaClČÜÓŚ1.00LĖ®ÖŠ£¬ĖłµĆNaClČÜŅŗµÄÅضČĪŖ1.00mol•L-1 | |
| C£® | 1molCl2Óė×ćĮæµÄĢś·“Ó¦£¬×ŖŅʵĵē×ÓŹżĪŖ3NA | |
| D£® | 1molAl3+ŗ¬ÓŠµÄŗĖĶāµē×ÓŹżĪŖ3NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 10mL 20mL | B£® | 20mL 30mL | C£® | 10mL 36.7mL | D£® | 20mL 36.7mL |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ė®µēĄė³öµÄc£ØH+£©=1.0”Į10-13mol/LµÄČÜŅŗÖŠ£¬Na+”¢NH4+”¢Cl-”¢SO42- | |
| B£® | µĪČė¼×»ł³ČŹŌŅŗ±äŗģÉ«µÄČÜŅŗÖŠ£ŗCl-”¢AlO2-”¢HCO3-”¢NH4+ | |
| C£® | ¼ÓČėÉŁĮæKSCNŗó±äĪŖŗģÉ«µÄČÜŅŗÖŠ£ŗK+”¢Mg2+”¢I-”¢NO3- | |
| D£® | ĪŽÉ«ĶøĆ÷µÄČÜŅŗÖŠ£ŗCH3COO-”¢CO32-”¢K+”¢Na+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | -1131.2 | B£® | -647.6 | C£® | -507.8 | D£® | -323.8 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1 mol±½¼×ĖįŌŚÅØH2SO4“ęŌŚĻĀÓė×ćĮæŅŅ“¼·“Ó¦æɵĆ1 mol±½¼×ĖįŅŅõ„ | |
| B£® | 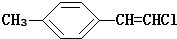 ·Ö×ÓÖŠµÄĖłÓŠŌ×ÓÓŠæÉÄܹ²Ę½Ćę ·Ö×ÓÖŠµÄĖłÓŠŌ×ÓÓŠæÉÄܹ²Ę½Ćę | |
| C£® | ·Ö×ÓŹ½ĪŖC5H12OµÄ“¼£¬ÄÜŌŚĶ“ß»ÆĻĀ±»O2Ńõ»ÆĪŖČ©µÄĶ¬·ÖŅģ¹¹ĢåÓŠ4ÖÖ | |
| D£® | 1 mol°¢Ė¾Ę„Į֣ؽį¹¹¼ņŹ½¼ūĶ¼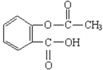 £©Óė×ćĮæµÄĒāŃõ»ÆÄĘČÜŅŗ¼ÓČČ·“Ó¦£¬×ī¶ąĻūŗĵÄĒāŃõ»ÆÄʵÄĪļÖŹµÄĮæ2 mol £©Óė×ćĮæµÄĒāŃõ»ÆÄĘČÜŅŗ¼ÓČČ·“Ó¦£¬×ī¶ąĻūŗĵÄĒāŃõ»ÆÄʵÄĪļÖŹµÄĮæ2 mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| Ń”Ļī | ŹµŃé²Ł×÷ | ŹµŃéÄæµÄ |
| A | ĻņĖ®½āŗóµÄÕįĢĒČÜŅŗÖŠÖ±½Ó¼ÓČėŠĀÖʵÄCu£ØOH£©2²¢¼ÓČČ | Č·¶ØÕįĢĒŹĒ·ń·¢ÉśĖ®½ā |
| B | µĪ¼ÓKMnO4£ØH+£©ČÜŅŗ£¬³ä·ÖÕńµ“ | Č·¶Ø±½ÖŠ»ģÓŠ¼ŗĻ© |
| C | ¼ÓČė½šŹōÄĘ | Č·¶Ø¾Ę¾«ÖŠ»ģÓŠ“×Ėį |
| D | ¼Óµķ·Ū | Č·¶ØKClÖŠŗ¬ÓŠKI |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com