
| ||
| ��t |
| ||
| 8 |
| 3 |
| 8 |
| 1 |
| 3 |
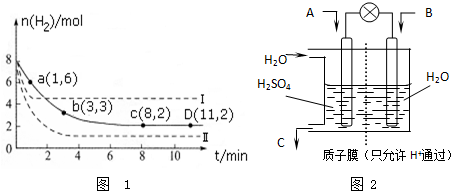
| 6mol |
| 2L |
| 1��1 |
| 2��13 |


 ������ϵ�д�
������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����͡����ͺ�ֲ���Ͷ���̼�⻯���� |
| B���ɼ�����ȴ�����4�֣�����֪������ȴ�����6�� |
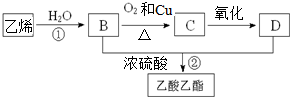
| C����ϩ�ͱ���������ʹ��ˮ��ɫ�����ܼ�����ϩ�ͱ����� |
| D�������£���������Br2��Ӧ����һ��ȡ����ֻ��һ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
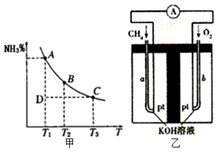 ���û�ѧ��Ӧԭ���о�̼�����ĵ��ʼ��仯����ķ�Ӧ������Ҫ���壮
���û�ѧ��Ӧԭ���о�̼�����ĵ��ʼ��仯����ķ�Ӧ������Ҫ���壮| c(H+) |
| c(OH-) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����NaAlO2��Һ�м������������Һ |
| B����AlCl3��Һ�м��������ˮ |
| C����AlCl3��Һ�м������NaOH��Һ |
| D����Al2O3��ˮ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 �����dzµ��㡱��������Ϊ���ڴ������������������ζ��������������ʵ��������Ҳ��������ͼ��ʾ��װ����ȡ�����������ش��������⣺
�����dzµ��㡱��������Ϊ���ڴ������������������ζ��������������ʵ��������Ҳ��������ͼ��ʾ��װ����ȡ�����������ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���� | ���� | ʵ������ | ���� |
| �� | ȡ��������ˮ������ҺX ���뼸��KSCN��Һ | ��ҺX�ʻ�ɫ������ֺ�ɫ | X���� |
| �� | ȡ������ҺX�������Ȼ� ����Һ���������ɳ��������� | �ϲ���ҺΪ��ɫ ���ɰ�ɫ���� | X���ܺ��� |
| �� | ȡ�������ɰ�ɫ����������ϡ���� | �������ܽ� | |
| �� | ȡ�����ϲ���Һ��������������Һ | ���ɰ�ɫ���� | X����Cl- |
| ���ۣ��˰�ɫ��������� | |||
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com