
 以图中A→K是中学化学中常见的物质,其中A、C、E是金属,F、G为气体单质,其余均为化合物,C焰色反应呈黄色,D为红棕色粉末,K为红褐色固体.
以图中A→K是中学化学中常见的物质,其中A、C、E是金属,F、G为气体单质,其余均为化合物,C焰色反应呈黄色,D为红棕色粉末,K为红褐色固体.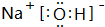 ,故答案为:
,故答案为: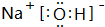 ;
;
| ||
| ||


 金钥匙试卷系列答案
金钥匙试卷系列答案科目:高中化学 来源: 题型:
| A、Ba(OH)2与HCl的中和反应 |
| B、葡萄糖在人体内氧化分解 |
| C、Ba(OH)2?8H20与NH4Cl反应 |
| D、锌粒与稀H2S04反应制取H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图是一些常见的单质和化合物之间的转化关系图,有些反应中的部分物质被略去.常温常压下,A为无色有毒气体,B为红棕色粉末,C、E为金属单质.反应①、②均为工业上的重要反应.
如图是一些常见的单质和化合物之间的转化关系图,有些反应中的部分物质被略去.常温常压下,A为无色有毒气体,B为红棕色粉末,C、E为金属单质.反应①、②均为工业上的重要反应.查看答案和解析>>
科目:高中化学 来源: 题型:
 两组同学对碳酸钠和碳酸氢钠的混合物与酸的反应进行探究.
两组同学对碳酸钠和碳酸氢钠的混合物与酸的反应进行探究.
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验要求 | 化学试剂 | 现象 |
| 酒精(水) | ||
| 味精(小苏打) | ||
| 蔗糖(葡萄糖) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验操作 | 答案 | 实验现象 |
| (1)将浓硫酸滴在小木条上 | A.产生白烟 | |
| (2)将分别蘸有浓氨水和浓盐酸的玻璃棒靠近 | B.产生蓝色物质 | |
| (3)在盛有KI淀粉溶液的试管中滴加氯水 | C.溶液呈红色 | |
| (4)在盛有FeC13溶液的试管中滴入2滴KSCN溶液 | D.变黑色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、10℃,5mL 3%H2O2溶液 |
| B、10℃,5mL 5%H2O2溶液 |
| C、30℃,5mL 5%H2O2溶液 |
| D、30℃,5mL 5%H2O2溶液且加入少量MnO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com