
【题目】下列操作中不能使指定物质或粒子的浓度增大的是( )
A.向AgCl悬浊液中加入少量Na2S固体,使溶液中Cl-浓度增大
B.向新制氯水中加入少量大理石,使HClO浓度增大
C.压缩平衡体系2NO2![]() N2O4的体积,使NO2浓度增大
N2O4的体积,使NO2浓度增大
D.向Fe(NO3)2溶液中,加入少量盐酸抑制Fe2+的水解,使Fe2+浓度增大
【答案】D
【解析】
A.AgCl悬浊液中存在平衡AgCl(s)![]() Ag+(aq)+Cl-(aq),加入的Na2S固体溶于水电离产生的S2-与Ag+结合生成更难溶的Ag2S沉淀,导致上述平衡右移,Cl-浓度增大,A不符合题意;
Ag+(aq)+Cl-(aq),加入的Na2S固体溶于水电离产生的S2-与Ag+结合生成更难溶的Ag2S沉淀,导致上述平衡右移,Cl-浓度增大,A不符合题意;
B.酸性:盐酸>碳酸>次氯酸,氯水中存在平衡Cl2+H2O![]() HCl+HClO,加入的大理石(CaCO3)与盐酸反应,使上述平衡右移,HClO浓度增大,B不符合题意;
HCl+HClO,加入的大理石(CaCO3)与盐酸反应,使上述平衡右移,HClO浓度增大,B不符合题意;
C.缩小体积后,平衡体系2NO2![]() N2O4中各物质的浓度均增大,平衡虽向右移动,但平衡移动的结果不会抵消条件的改变而引起的浓度增大,C不符合题意;
N2O4中各物质的浓度均增大,平衡虽向右移动,但平衡移动的结果不会抵消条件的改变而引起的浓度增大,C不符合题意;
D.NO3-在酸性条件下具有强氧化性,能将Fe2+氧化为Fe3+,溶液中Fe2+会减小,D符合题意;
答案选D。


科目:高中化学 来源: 题型:
【题目】在一次有机化学课堂小组讨论中,某同学设计了下列合成路线,你认为不可行的是( )
A.用氯苯合成环己烯: ![]()
B.用甲苯合成苯甲醇: ![]()
C.用乙烯合成乙酸: C2H4![]() CH3CH2OH
CH3CH2OH![]() CH3CHO
CH3CHO![]() CH3COOH
CH3COOH
D.用乙烯合成乙二醇: H2C=CH2![]() CH3CH3
CH3CH3![]() CH2ClCH2Cl
CH2ClCH2Cl![]() HOCH2CH2OH
HOCH2CH2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图装置进行实验,将液体A逐滴加入到固体B中,下列叙述正确的是( )
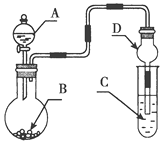
A.若A为浓盐酸,B为KMnO4晶体,C中盛有紫色石蕊溶液,则C中溶液最终呈红色
B.实验仪器D可以起到防止溶液倒吸的作用
C.若A为浓氨水,B为生石灰,C中盛有AlCl3溶液,则C中溶液先产生白色沉淀后沉淀又溶解
D.若A为浓H2SO4,B为Cu,C中盛有澄清石灰水,则C中溶液变浑浊
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A与B是短周期的两种元素,它们的离子![]() 与
与![]() 具有相同的核外电子层结构,则下列说法中正确的是( )
具有相同的核外电子层结构,则下列说法中正确的是( )
A.原子序数A>BB.电子数A>BC.原子半径A>BD.离子半径![]() >
>![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物。

完成下列各题:
(1)正四面体烷的分子式为__________________。
(2)关于乙烯基乙炔分子的说法错误的是:_________。
a. 能使酸性![]() 溶液褪色
溶液褪色
b. 1mol乙烯基乙炔能与3mol![]() 发生加成反应
发生加成反应
c. 乙烯基乙炔分子内含有两种官能团
d. 等质量的乙炔与乙烯基乙炔完全燃烧时耗氧量不相同
(3)1866年凯酷勒提出了苯的单、双键交替的正六边形平面结构,解释了苯的部分性质,但还有一些问题尚未解决,它不能解释下列_________事实(填入编号)。
a. 苯不能使溴水褪色 b. 苯能与![]() 发生加成反应
发生加成反应
c. 溴苯没有同分异构体 d. 邻二溴苯只有一种
(4)写出与环辛四烯互为同分异构体且属于芳香烃的分子的结构简式:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烯是重要的化工原料,工业上以丙烯为原料可合成高分子化合物F和香料K,其流程如图所示:
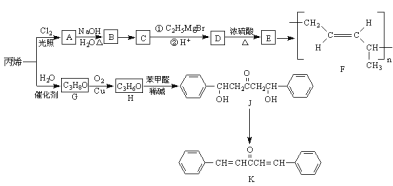
已知: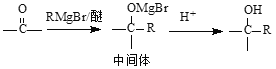 (R为烃基)
(R为烃基)
(1)G的名称为___,J中含氧官能团的名称为___。
(2)由D生成E的反应类型为___;由H生成J的反应类型为___。
(3)已知A中只含有1个氯原子,写出由A生成B的化学方程式___。
(4)由K可合成另外一种香料M(![]() ),M的分子式为___,M的芳香同分异构体中能发生水解反应和银镜反应的有___种,其中核磁共振氢谱有4组峰的同分异构体的结构简式为___。
),M的分子式为___,M的芳香同分异构体中能发生水解反应和银镜反应的有___种,其中核磁共振氢谱有4组峰的同分异构体的结构简式为___。
(5)利用“![]() ”为初始原料合成
”为初始原料合成![]() ,写出合成路线___(其它无机试剂任选)。
,写出合成路线___(其它无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化亚铜(Cu2O)是一种用途广泛的光电材料,某工厂以硫化铜矿石(含 CuFeS2、Cu2S等)为原料制取Cu2O的工艺流程如下:
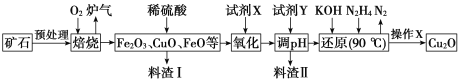
常温下几种物质开始形成沉淀与完全沉淀时的pH如下表:
Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
开始沉淀 | 7.5 | 2.7 | 4.8 |
完全沉淀 | 9.0 | 3.7 | 6.4 |
(1)炉气中的有害气体成分是___________,Cu2S与O2反应时,氧化剂与还原剂的物质的量之比为___________。
(2)试剂X是H2O2溶液,当试剂X是___________时,更有利于降低生产成本。
(3)加入试剂Y调pH时,pH的调控范围是________。
(4)“还原”步骤中为提高N2H4转化率可采取的措施有_________(填序号)。
a.不断搅拌,使N2H4和溶液充分接触 b.增大通入N2H4的流速
c.减少KOH的进入量 d.减小通入N2H4的流速
(5)写出用N2H4制备Cu2O的化学方程式为_______________
(6)操作X包括烘干,其中烘干时要隔绝空气,其目的是____________。
(7)以铜与石墨作电极,电解浓的强碱性溶液可制得纳米级Cu2O,写出阳极上生成Cu2O的电极反应式为________
(8)工业上用氨气生产氢氰酸(HCN的反应为:CH4(g)+NH3(g)HCN(g)+3H2(g ) △H>0。其他条件一定,达到平衡时NH3转化率随外界条件X变化的关系如图所示。则X可以是___________(填字母序号)
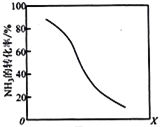
a.温度 b.压强 c.催化剂 d.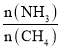
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物 K 是某药物的中间体,合成路线如图所示:
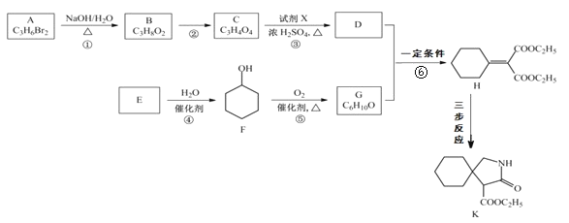
已知:i.R-CN![]() R-CH2-NH2
R-CH2-NH2
ii.R1-NH2+R2COOC2H5![]()
![]() +C2H5OH
+C2H5OH
回答下列问题
(1)A 的名称是_______。
(2)反应①的化学方程式是_____。
(3)反应②的类型是_____。
(4)反应③中的试剂 X是_____。
(5)E 属于烃,其结构简式是_____。
(6)H 中所含的官能团是_____。
(7)反应⑥的化学方程式是_____。
(8)H 经三步反应合成 K:H![]() I→J→K,写出中间产物 I和J的结构简式_____。
I→J→K,写出中间产物 I和J的结构简式_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制物质的量浓度为0.1 mol·L-1的Na2CO3溶液100 mL时,下列操作正确的是( )
A. 用托盘天平称取1.06 g无水碳酸钠,在烧杯中加适量水溶解,待冷却到室温后,将溶液转移到容量瓶中
B. 在使用容量瓶前必须检查容量瓶是否完好以及瓶塞处是否漏水
C. 定容时,若加水超过刻度线,可用胶头滴管小心吸出多余部分
D. 定容时,若仰视,则所配溶液的浓度将偏高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com