
【题目】肉桂皮是肉桂树的树皮,常被用作药物和食用香料,有效成分为肉桂醛。从肉桂皮中提取肉桂醛的主要流程如下:

下列说法不正确的是
A.肉桂醛可用作食品添加剂且不应过量
B.肉桂醛可溶于乙醇
C.红外光谱可检测出肉桂醛分子中含有碳碳双键和醛基
D.肉桂醛长期置于空气中容易发生还原反应
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:高中化学 来源: 题型:
【题目】含氮化合物对环境、生产和人类生命活动等具有很大的影响。请按要求回答下列问题
(1)利用某分子筛作催化剂,NH3可脱除工厂废气中的NO、NO2,反应机理如下图所示。A包含物质为H2O和___________(填化学式)

(2)已知:4NH3(g)+6NO(g) =5N2(g)+6H2O(g) △H1=-a kJ/mol
4NH3(g)+5O2(g)= 4NO(g)+6H2O(g) △H2=-b kJ/mol
H2O(l)=H2O(g) △H3=+c kJ/mol
则反应4NH3(g)+3O2(g)=2N2(g)+6H2O(l)的△H=___________ kJ/mol
(3)工业上利用氨气生产氢氰酸(HCN的反应为:CH4(g)+NH3(g)![]() HCN(g)+3H2(g ) △H>0
HCN(g)+3H2(g ) △H>0
①其他条件一定,达到平衡时NH3转化率随外界条件X变化的关系如图甲所示。则X可以是___________(填字母序号)

a.温度 b.压强 c.催化剂 d.![]()
②在一定温度下,向2L密闭容器中加入 n mol CH4和2 moI NH3,平衡时NH3体积分数随n变化的关系如图乙所示。

a点时,CH4的转化率为___________%;平衡常数:K(a)_____K(b)(填“>”“=”或“<”)。
(4)肌肉中的肌红蛋白(Mb)与O2结合生成MbO2,其反应原理可表示为: Mb(ag)+O2(g)![]() MbO2(aq),该反应的平衡常数可表示为:
MbO2(aq),该反应的平衡常数可表示为:![]() 。在37℃条件下达到平衡时,测得肌红蛋白的结合度(a)与P(O2)的关系如图丙所示[
。在37℃条件下达到平衡时,测得肌红蛋白的结合度(a)与P(O2)的关系如图丙所示[![]() ]。研究表明正反应速率ν正=k正·c(Mb) · P(O2),逆反应速率ν逆=k逆·c(MbO2)(其中k正和k逆分别表示正反应和逆反应的速率常数)。
]。研究表明正反应速率ν正=k正·c(Mb) · P(O2),逆反应速率ν逆=k逆·c(MbO2)(其中k正和k逆分别表示正反应和逆反应的速率常数)。

①试写出平衡常数K与速率常数k正、k逆之间的关系式为K=___________(用含有k正、k逆的式子表示)。
②试求出图丙中c点时,上述反应的平衡常数K=___________kPa-1。已知k逆=60s-1,则速率常数k正=___________s-1·kPa-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前的锂离子电池的正极材料多是LiCoO2、LiMn2O4、LiFePO4和双离子传递型聚合物等。改良正极材料的性能是锂离子电池领域的重点方向,如用碳包覆LiFePO4和向其中掺杂金属银等。下列过程是制备该正极材料的流程图:
![]()
回答下列问题:
(1)LiFePO4中铁元素的化合价为_____价。已知原料是Li2CO3、FeC2O4·2H2O、NH4H2PO4和C6H12O6的混合物,其中Li、Fe、P三种元素的物质的量比为1:1:1,C6H12O6的用量占原料总质量的5%。若原料的质量为1000 g,则需要称取NH4H2PO4的质量为_______(保留两位小数)。
(2)将原料先行研磨4 h目的是_________。为了更快得到前驱体粉末,除了保持温度在50℃外,还应进行的常见操作方法是_________。
(3)两次焙烧均需要在高纯氮气环境下进行,原因是________。葡萄糖分解产生的碳除了提供还原性环境,提高产物纯度,而且可以阻止晶粒的聚集长大,控制颗粒形状,提高LiFePO4的电导率。则葡萄糖分解的化学反应方程式(分解过程中只有C一种单质生成)为________。600℃加热时硝酸银发生分解生成红棕色气体和3种常见单质(其中两种气体单质物质的量比为2:7),则分解时的化学反应方程式为_______。
(4)如图所示是用LiFePO4/Ag/C作正极材料制成的纽扣锂离子电池组装示意图。充电时,其正、负极材料所发生反应的电极方程式分别是______、______(锂离子电池是靠xLi+在两极的嵌入和嵌出进行工作)。
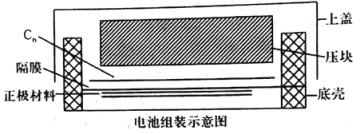
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石油加氢精制和天然气净化等过程产生有毒的H2S,直接排放会污染空气。
(1)工业上用克劳斯工艺处理含H2S的尾气获得硫黄,流程如下:
![]()
①反应炉中的反应:2H2S(g)+3O2(g) =2SO2(g)+2H2O(g) H=-1035.6 kJ·mol1
催化转化器中的反应:2H2S(g)+SO2(g) = 3S(g)+2H2O(g) H=-92.8 kJ·mol1
克劳斯工艺中获得气态硫黄的总反应的热化学方程式:______。
②为了提高H2S转化为S的比例,理论上应控制反应炉中H2S的转化率为______。
(2)科研工作者利用微波法处理尾气中的H2S并回收H2和S,反应为:H2S![]() H2+S,一定条件下,H2S的转化率随温度变化的曲线如图。
H2+S,一定条件下,H2S的转化率随温度变化的曲线如图。
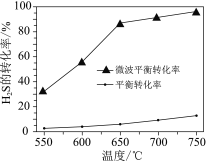
①H2S分解生成H2和S的反应为______反应(填“吸热”或“放热”)。
②微波的作用是______。
(3)某科研小组将微电池技术用于去除天然气中的H2S,装置示意图如下,主要反应:2Fe+2H2S+O2= 2FeS+2H2O(FeS难溶于水),室温时,pH=7的条件下,研究反应时间对H2S的去除率的影响。

①装置中微电池负极的电极反应式:______。
②一段时间后,单位时间内H2S的去除率降低,可能的原因是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一个铝制易拉罐充满![]() 后,再往罐内注入足量的
后,再往罐内注入足量的![]() 溶液,立即用胶布严封罐口,不多会儿就会听到罐内“咔、咔”作响,发现易拉罐变瘪,再过一会儿易拉罐又鼓涨起来,解释上述变化的实验现象.
溶液,立即用胶布严封罐口,不多会儿就会听到罐内“咔、咔”作响,发现易拉罐变瘪,再过一会儿易拉罐又鼓涨起来,解释上述变化的实验现象.
(1)易拉罐开始变瘪的原因是___________,其离子方程式(或化学方程式)为___________.
(2)易拉罐后来又鼓涨起来的原因是_____________,其离子方程式(或化学方程式)为_______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将10 mL充满NO2和O2的混合气体的试管,倒置在水槽中,反应停止后试管内剩余2 mL的无色气体,求原混合气体中NO2和O2各多少毫升____________?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏伽德罗常数的数值,下列叙述正确的是
A. 78g苯中含有的碳碳双键的数目为3NA
B. 16gCu2S和CuO组成的混合物中含有的阳离子数为0.2NA
C. 将1mol H2与 1 mol I2充入一密闭容器中充分反应后,转移的电子书为2NA
D. 1 mol Fe 与足量的浓硫酸共热反应,生成SO2的分子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中浓度关系正确的是
A.小苏打溶液中:c(Na+)+c(H+)=c(![]() )+c(
)+c(![]() )+c(OH-)
)+c(OH-)
B.CH3COONa溶液中:c(CH3COO-) > c(Na+) > c(OH-) > c(H+)
C.0.1 mol/L的NaHA溶液,其pH=4,则c(HA-)>c(H+)>c(H2A)>c(A2-)
D.物质的量浓度相等的CH3COOH溶液和CH3COONa溶液等体积混合:c(CH3COO-)+2c(OH-)=2c(H+)+c(CH3COOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】普通水泥在固化过程中自由水分子减少并产生Ca(OH)2,溶液呈碱性。根据这一物理化学特点,科学家发明了电动势法测水泥初凝时间。此方法的原理如图所示,反应的总方程式为:2Cu+Ag2O=Cu2O+2Ag,下列有关说法正确的

A.Cu为正极,Ag2O为负极
B.电池工作时,OH—向正极移动
C.正极的电极反应为:2Cu+2OH——2e—=Cu2O+H2O
D.外电路中每通过2mol电子,正极质量减少16g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com