
【题目】已知断裂1molC﹣H键,要吸收热量414.4kJ;断裂1mol C﹣C键,要吸收热量347.4kJ;生成1mol C═C键,会放出热量615.3kJ;生成1mol H﹣H键,会放出热量435.3kJ,某有机物分解的反应可表示为: 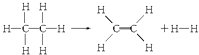
若在反应中消耗了1mol乙烷(反应物),则有关该反应的说法正确的是( )
A.该反应放出251.2 kJ的热量
B.该反应吸收251.2 kJ的热量
C.该反应放出125.6 kJ的热量
D.该反应吸收125.6 kJ的热量
科目:高中化学 来源: 题型:
【题目】请回答下列问题:
(1)火箭燃料液态偏二甲肼(C2H8N2)是用液态N2O4作氧化剂,二者反应放出大量的热,生成无毒、无污染的气体和水.已知室温下,1g燃料完全燃烧释放出的能量为42.5kJ,则该反应的热化学方程式为 .
(2)298K时,在2L固定体积的密闭容器中,发生可逆反应:2NO2(g)N2O4(g)△H=﹣akJmol﹣1 (a>0).N2O4的物质的量浓度随时间变化如图1.达平衡时,N2O4的浓度为NO2的2倍,回答下列问题:
①298k时,该反应的平衡常数为Lmol﹣1(精确到0.01).
②下列情况不是处于平衡状态的是:
a.混合气体的密度保持不变;b.混合气体的颜色不再变化; c.气压恒定时.
③若反应在398K进行,某时刻测得n(NO2)=0.6mol n(N2O4)=1.2mol,则此时V(正)V(逆)(填“>”、“<”或“=”).
(3)工业上“除钙、镁”的原理反应为:MgSO4+2NaF═MgF2↓+Na2SO4;CaSO4+2NaF═CaF2↓+Na2SO4
已知KSP(CaF2)=1.11×10﹣10 , KSP(MgF2)=7.40×10﹣11 , 加入过量NaF溶液反应完全后过滤,则滤液中 ![]() = .
= .
(4)电解法可消除甲醇对水质造成的污染,原理是:通电将Co2+氧化成Co3+ , 然后Co3+将甲醇氧化成CO2和H+(用石墨烯吸附除去Co2+).现用图2装置模拟上述过程,则:Co2+在阳极的电极反应式为:;
除去甲醇的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在溶液中可进行反应A+B![]() C+D,其中A、B在一定条件下反应并测定反应中生成物C的浓度随反应时间的变化情况,绘制出如图所示的图线。(0~t1、t1~t2、t2~t3各时间段相同)下列说法不正确的是
C+D,其中A、B在一定条件下反应并测定反应中生成物C的浓度随反应时间的变化情况,绘制出如图所示的图线。(0~t1、t1~t2、t2~t3各时间段相同)下列说法不正确的是

A. 该反应是吸热反应
B. 反应速率最大的时间段是在t1~t2
C. 四个时间段内生成C的量最多的是t1~t2
D. 反应速率后来减慢主要是受反应物浓度变化的影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2O2是常用的绿色氧化剂,H2S是还原剂,但H2S会对环境和人体健康带来极大危害。
I.H2S的除去,生物脱H2S的原理为:H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4、4FeSO4+O2+2H2SO4![]() 2Fe2(SO4)3+2H2O。
2Fe2(SO4)3+2H2O。
(1)硫杆菌存在时,FeSO4被氧化的速率是无菌时的5×105倍,该菌的作用是_____。
(2)由图甲和图乙判断他用硫杆菌的最佳条件为_______。在最佳条件下,该反应的加热方式为_________,若反应温度过高,反应速率下降,其原因是__________。

II.为研究硫酸饮的量对过氧化氢分解速率的影响,某同学设计了如下一系列的实验。将表中所给的溶液分别加入A、B、C、D四个反应瓶中,收集产生的气体,在关数据如下:
实验溶液 | A/mL | B/mL | C/mL | D/mL |
0.4mol/LFe2(SO4)3溶液 | 0 | 1.0 | 2.0 | V1 |
30%H2O2溶液 | V2 | 20.0 | 20.0 | 20.0 |
H2O | 18.0 | 17.0 | V3 | 15.0 |
(1)实验过程中需记录的数据是___________。
(2)上表中的V2=_______,V3=_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应:2NO2 ![]() 2NO+O2在体积固定的密闭容器中,达到平衡状态的标志是( ) ①单位时间内生成n mol O2的同时生成2n mol NO2
2NO+O2在体积固定的密闭容器中,达到平衡状态的标志是( ) ①单位时间内生成n mol O2的同时生成2n mol NO2
②单位时间内生成n mol O2的同时生成2n mol NO
③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2:2:1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的压强不再改变的状态
⑦混合气体的平均相对分子质量不再改变的状态.
A.①④⑥⑦
B.②③⑤⑦
C.①③④⑤
D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有四种化合物W,X,Y,Z,它们都是由短周期元素A,B,C,D,E中的两种元素组成的.已知: (a)A,B,C,D,E五种元素的原子序数依次增大,且A,D同主族,C,E同主族,B、C同周期.
(b)W由B,C组成,分子中原子个数比为B:C=1:2,固体易升华.
(c)X由A,C组成,分子中原子个数比为A:C=1:1.
(d)Y由C,D形成的离子化合物,且Y中相应元素的微粒之比为:C:D=1:1.
(e)Z是由D,E形成的离子化合物,其中阳离子比阴离子少一个电子层,阴、阳离子数之比为1:2.
试回答下列各小题:
(1)各元素符号:ABCDE
(2)W的电子式: .
(3)X的结构式: .
(4)Y的电子式: .
(5)Z的化学式: .
(6)写出Y与水反应的化学方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无色的混合气体甲,可能含NO、CO2、NO2、NH3、N2中的几种,将100 mL甲气体经过下图实验的处理,结果得到酸性溶液,而几乎无气体剩余,则甲气体的组成为( )
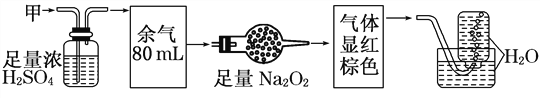
A. NH3、NO2、N2 B. NH3、NO、CO2
C. NH3、NO2、CO2 D. NO、CO2、N2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com