
环状结构(BHNH)3,称为无机苯,它和苯是等电子体,(BHNH)3的结构简式如图,试推测无机苯二氯代物共有多少种同分异构体( )
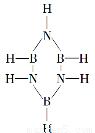
A.5种 B.4种
C.3种 D.2种
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2015-2016学年重庆四十二中高一下期中化学试卷(解析版) 题型:选择题
下列物质中既有离子键又有共价键的是( )
A.CaCl2 B.H2O C.K2O D.NaOH
查看答案和解析>>
科目:高中化学 来源:2015-2016学年海南省高一下学期期末考试化学试卷(解析版) 题型:选择题
下列叙述正确的是
A.电能是二次能源
B.水力是二次能源
C.天然气是二次能源
D.水煤气是一次能源
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高一下学期期末考试化学试卷(解析版) 题型:选择题
月球表面土壤里有1种非常有用的资源3He——可控核聚变的原料,有关叙述正确的是( )
A. 在3He中存在:质子数=中子数=核外电子数
B. 3He和4He是同种原子
C. 核聚变时,原子核发生了变化,发生了化学反应
D. 3He和4He互为同位素
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二下学期期末考试化学试卷(解析版) 题型:推断题
A、B都是芳香族化合物,1molA水解得到1molB和1mol醋酸。A、B的相对分子质量都不超过200,完全燃烧都只生成CO2和H2O。且B分子中碳和氢元素总的质量分数为65.2%。A溶液具有酸性,不能使FeCl3溶液显色。
(1)A、B的相对分子质量之差为 。
(2)1个B分子中应该有 个氧原子。
(3)A中所含的官能团名称: 。
(4)1molB物质分别与足量的碳酸氢钠溶液、氢氧化钠溶液反应理论上消耗二者的物质的量之比是 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二下学期期末考试化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列有关叙述不正确的是( )
A.1 mol碳正离子(CH3+)所含的电子总数为8 NA
B.1 mol甲基(—CH3)所含的电子总数为9NA
C.0.5mol 1, 3-丁二烯分子中含有碳碳双键数为 NA
D.标准状况下,1L庚烷完全燃烧所生成的气态产物的分子数为(7/22.4)NA
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二下学期期末考试化学试卷(解析版) 题型:选择题
有机物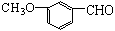 ,有多种同分异构体,其中属于酯且含有苯环结构的共有( )
,有多种同分异构体,其中属于酯且含有苯环结构的共有( )
A.3种 B.4种 C.5种 D.6种
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省扬州市高二选修下学期期末调研化学试卷(解析版) 题型:选择题
常温下,向0.1 mol·L-1CH3COOH溶液中不断加水,过程中始终保持增大的是
A.c(H+)
B.Ka(CH3COOH)
C.c(H+)•c(OH-)
D.c(H+)/c(CH3COOH)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年陕西西安高新一中高一下期末化学试卷(解析版) 题型:推断题
气相直接水合法制乙醇的方程式为:C2H4 (g)+H2O(g)=C2H5OH(g),其中乙烯的平衡转化率与温度、压强的关系如图[起始n(H2O)︰n(C2H4)=1︰1]。
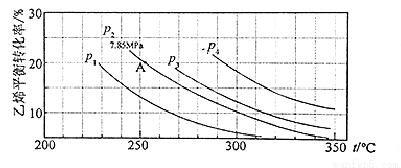
计算乙烯水合制乙醇反应在图中A点的平衡常数KP为(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
A.0.068 MPa-1 B.0.082 C.0.072 MPa-1 D.0.082 MPa-1
【答案】C
【解析】
试题分析:由图可知,A点乙烯的平衡转化率为20%,设起始量n(H2O)=n(C2H4)=1mol,转化的乙烯为0.2mol,则: C2H4 (g)+H2O(g)=C2H5OH(g)
起始量(mol):1 1 0
转化量(mol):0.2 0.2 0.2
平衡量(mol):0.8 0.8 0.2
压强之比等于物质的量之比,则p(C2H4)=p(H2O)=7.8MPa×(0.8mol÷1.8mol)=7.8MPa×4/9,p(C2H5OH)=7.8MPa×1/9,则Kp=p(C2H5OH)/[p(C2H4)×p(H2O)]=(7.8MPa×1/9)7.8MPa×4/9×7.8MPa×4/9 =0.072MPa-1,选项C正确。
考点:考查图像方法在化学平衡计算的应用的知识。
【题型】选择题
【适用】较难
【标题】【百强校】2015-2016学年陕西西安高新一中高一下期末化学试卷(带解析)
【关键字标签】
【结束】
X、Y、Z、J、Q五种短周期主族元素,原子序数依次增大,元素Z在地壳中含量最高,J元素的焰色反应呈黄色,Q的最外层电子数与其电子总数比为3:8,X能与J形成离子化合物,且J+的半径大于X-的半径,Y2是空气的主要成分之一。请回答:
(1)Q元素在周期表中的位置_______________________;
(2)这五种元素原子半径从大到小的顺序为_____________________________(填元素符号)。
(3)元素的非金属性Z____Q(填“>”或“<”),下列各项中,不能说明这一结论的事实有 (填序号)
A.Q的氢化物的水溶液放置在空气中会变浑浊 |
B.Z与Q之间形成的化合物中元素的化合价 |
C.Z和Q的单质的状态 |
D.Z和Q在周期表中的位置 |
(4)X与Y可形成简单分子A,写出A的电子式_______________;实验室制备气体A的化学方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com