
【题目】根据下列实验事实得出的相应结论正确的是( )
选项 | 实验事实 | 结论 |
A | NH3 的水溶液可以导电 | NH3 是电解质 |
B | SO2 通入硝酸钡溶液出现白色沉淀 | BaSO3 不溶于强酸 |
C | 浓硝酸久置发黄 | 硝酸不稳定 |
D | 浓硫酸能脱去胆矾晶体中的水 | 浓硫酸具有脱水性 |
A.AB.BC.CD.D
【答案】C
【解析】
A. NH3 的水溶液可以导电是因为:NH3 + H2O ![]() NH3H2O, NH3H2O
NH3H2O, NH3H2O ![]() NH4+ + OH-,并不是NH3 自身电离导致的,所以NH3 是非电解质,A选项错误;
NH4+ + OH-,并不是NH3 自身电离导致的,所以NH3 是非电解质,A选项错误;
B. SO2 通入硝酸钡溶液出现白色沉淀,是因为SO2被NO3-氧化成SO42-,并进一步生成了BaSO4沉淀,B选项错误;
C. 浓硝酸久置发黄是因为:4HNO3 = 4NO2↑ + O2↑ + 2H2O,体现了硝酸的不稳定性,C选项正确;
D. 浓硫酸能脱去胆矾晶体中的水,体现的是浓硫酸的吸水性,原因是胆矾中的水是以H2O的形式与Cu2+和SO42-结合,而不是在脱水过程中形成的,D选项错误;
答案选C。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案科目:高中化学 来源: 题型:
【题目】有一种水果香精乙酸正丁酯的合成提纯步骤如下:
(1)合成:在干燥的圆底烧瓶中加11.5mL(9.3g,0.125mol)正丁醇 、3~4滴浓H2SO4、7.2mL(7.5g,0.125mol)冰醋酸,摇匀后,加几粒沸石,再按图1所示装置安装好。在分水器(分离出生成的水)中预先加入5.00mL水,其水面低于分水器回流支管下沿3~5mm,然后用小火加热,反应大约40min。
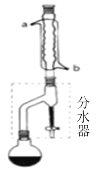
(2)分离提纯:
① 当分水器中的液面不再升高时,冷却,从分水器下端放出分水器中的水,把反应后的烧瓶中的溶液与分水器中的酯层合并,转入分液漏斗中,用10mL10%碳酸钠溶液洗至酯层无酸性(pH=7),充分震荡后静置,分去水层。
② 将酯层倒入小锥形瓶中,加少量无水硫酸镁干燥(生成MgSO47H2O晶体)。
③ 将乙酸正丁酯粗产品转入50mL图中的仪器中,加几粒沸石进行加热,收集产品,主要试剂及产物的物理常数如下:
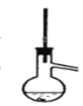
化合物 | 正丁醇 | 冰醋酸 | 乙酸正丁酯 | 正丁醚 |
密度/(g/mL) | 0.810 | 1.049 | 0.882 | 0.7689 |
沸点/℃ | 117.8 | 118.1 | 126.1 | 143 |
在水中的溶解性 | 易溶 | 易溶 | 难溶 | 难溶 |
制备过程中还可能存在的副反应有:2CH3CH2CH2CH2OH![]() CH3CH2CH2CH2OCH2CH2CH2CH3+H2O。根据以上信息回答下列问题:
CH3CH2CH2CH2OCH2CH2CH2CH3+H2O。根据以上信息回答下列问题:
(1)写出合成乙酸正丁酯的化学方程式_________。
(2)步骤①中碳酸钠溶液的作用主要是___________,若改用NaOH溶液洗涤酯层,收集到的产物比预期少,原因是:_____________。
(3)在操作步骤②后(即酯层用无水硫酸镁干燥后),应先___________(填实验操作名称),步骤③中加热分离有机物的实验方法名称是______________。
(4)步骤③的常压蒸馏,需控制一定的温度,你认为在______中加热比较合适(请从下列选项中选择)。
A.水 B.甘油(沸点290℃) C.沙子 D.石蜡油(沸点200~300℃)
(5)反应结束后,若放出的水为6.98mL(水的密度为1g/mL),则正丁醇的转化率约为:______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.实验室可用如下装置(略去部分夹持仪器)制取SO2并验证其性质。
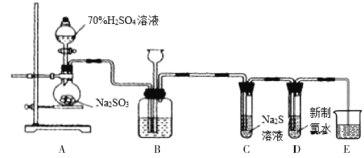
(1)盛装亚硫酸钠的仪器名称为________,若将亚硫酸钠改为铜片,与浓硫酸反应制取SO2,还缺少的仪器有_______,写出用铜片制取SO2的化学方程式_________________________。
(2)装置B的作用之一是通过观察产生气泡的多少判断SO2生成的快慢,其中的液体最好选择___________(填代号)。
a.饱和Na2CO3溶液 b.NaOH溶液 c.饱和NaHCO3溶液 d.饱和NaHSO3溶液
(3)验证SO2的还原性。取充分反应后装置D中的溶液,将其分成三份,分别进行如下实验:
方案I:第一份溶液中滴入AgNO3溶液,有白色沉淀生成;
方案II:第二份溶液中滴入品红溶液,红色褪去;
方案III:第三份溶液中滴入BaCl2溶液,产生白色沉淀。
上述方案合理的是___________(填“方案I”、“方案II”或“方案III”);对不合理的方案作出简要评价___________(如果认为都合理,可以不作答)。
II.已知2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O,若采用该方案制备Cl2并验证Cl2的性质。B、C、D中的试剂依次为:饱和食盐水、FeCl2溶液、石蕊溶液。
(4)C中反应的离子方程式为:_________________________________。
(5)D中可能观察到的现象为:_________________________________。
(6)装置E中盛放NaOH溶液,其目的是_________________________________,该反应的化学方程式是:_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯佐卡因是局部麻醉药,常用于手术后创伤止痛、溃疡痛等,其结构简式为 。下列关于苯佐卡因的叙述正确的是
。下列关于苯佐卡因的叙述正确的是
A. 分子式为C9H14NO2
B. 苯环上有2个取代基,且含有硝基的苯佐卡因的同分异构体有9种
C. 1mol该化合物最多与4mol氢气发生加成反应
D. 分子中将氨基转化成硝基的反应为氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图装置,将溶液 A 逐渐加入固体 B 中,下列叙述中不正确的是( )
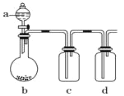
A.若 a 为浓盐酸,b 为 MnO2,c 中盛品红溶液,则 c 中溶液不褪色
B.若 a 为稀硫酸,b 为 FeS,c 中盛硫酸铜溶液,则 c 中产生淡黄色沉淀
C.若 a 为醋酸溶液,b 为贝壳,c 中盛过量澄清石灰水,则 c 中溶液变浑浊
D.若 a 为浓氨水,b 为生石灰,c 中盛 AlCl3 溶液,则 c 中产生白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分:(不得用a~h字母回答)元素周期表有7个横行,每一个横行称为“周期”,周期序数=电子层数;元素周期表共有18列,每一列称为 “族”,下表中的7列为主族元素,分别用罗马数字Ⅰ、Ⅱ、……表明族序数,族序数=最外层电子数。
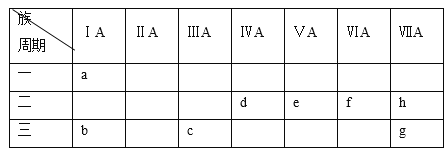
根据a~h各元素的性质,选择相应的化学符号、化学式或化学方程式填空:
(1)单质氧化性最强的是__________,酸性最强的含氧酸是_____________。
(2)写出e的碱性气态氢化物的电子式_____,将它和化合物df 2通入饱和食盐水发生反应的化学方程式是_____。
(3)最高价氧化物对应的水化物中,碱性最强的是___________。
(4)在b、c、g、h中,常见离子半径最大的是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是![]()
![]()
A.海水淡化的常用方法有蒸馏法、电渗析法和过滤法
B.pH相等的三种溶液:![]() 溶液
溶液![]() 溶液
溶液![]() 溶液,其浓度大小顺序为
溶液,其浓度大小顺序为![]()
C.在![]() 和
和![]() 的混合溶液中加入
的混合溶液中加入![]() 产生黑色沉淀,证明
产生黑色沉淀,证明![]()
D.侯式制碱法的化学方程式为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列有关叙述不正确的是( )
A. 标准状况下,1L庚烷完全燃烧所生成的气态产物的分子数为(7/22.4)NA
B. 1 mol甲基(-CH3)所含的电子总数为9NA
C. 0.5 mol1,3-丁二烯分子中含有碳碳双键数为NA
D. 1 mol碳正离子(CH3+)所含的电子总数为8NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中草药秦皮中含有的七叶树内酯(每个折点表示一个碳原子,氢原子未画出),具有抗菌作用.若1mol七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为( )
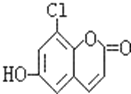
A.2molBr2、2molNaOHB.3molBr2、4molNaOH
C.3molBr2、5molNaOHD.4molBr2、5molNaOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com