
【题目】乙烯催化氧化成乙醛可设计成如图所示的燃料电池,在制备乙醛的同时能获得电能,其总反应为:2CH2═CH2+O2→2CH3CHO.下列有关说法不正确的是( ) 
A.该电池可将化学能转化为电能
B.每有0.1 mol O2反应,则迁移0.4 mol H+
C.正极反应式为:CH2=CH2﹣2e﹣+2OH﹣═CH3CHO+H2O
D.负极区溶液的pH减小
【答案】C
【解析】解:A.原电池工作时,将化学能转化为电能,故A正确;B.由电极方程式O2+4H++4e﹣═2H2O可知,每有0.1molO2反应,则迁移H+0.4mol,故B正确;
C.正极发生还原反应,电极方程式为O2+4H++4e﹣═2H2O,负极为CH2=CH2﹣2e﹣+H2O=CH3CHO+2H+ , 故C错误;
D.负极反应为CH2=CH2﹣2e﹣+H2O=CH3CHO+2H+ , 氢离子浓度增大,溶液的pH减小,故D正确;
故选C.
由总反应式可知CH2=CH2被氧化,应为原电池的负极反应,因电解质溶液呈酸性,则负极电极方程式为CH2=CH2﹣2e﹣+H2O=CH3CHO+2H+ , 正极通入氧气,发生还原反应,电极方程式为O2+4H++4e﹣═2H2O,以此解答该题.


科目:高中化学 来源: 题型:
【题目】利用处理废弃的线路板得到含70%Cu、25%Al、4%Fe及少量Au、Pt的金属混合物制备硫酸铜和硫酸铝晶体,流程如图1: 
(1)步骤①~③中过滤操作所需要的玻璃仪器除烧杯、漏斗外还有 .
(2)步骤①中Cu发生的离子方程式为 , 此时该溶液中所有的金属阳离子是;步骤②中得到滤渣2的主要成分是(填化学式).
(3)滤渣3加适量稀硫酸溶解,将得到溶液进行:蒸发浓缩, , 过滤、洗涤,即得到硫酸铜晶体;由滤液3制备Al2(SO4)318H2O时,按化学反应顺序用到的试剂依次为 . (填序号)
①NaOH溶液 ②稀硫酸 ③氨水 ④二氧化碳
(4)在步骤(3)中,发生反应的第一个离子方程式是
(5)为测定制得硫酸铜晶体(CuSO4xH2O)中结晶水含量,取12.5g硫酸铜晶体进行加热分解,得到固体质量与温度的关系如图2.
已知加热过程中,硫酸铜晶体分步失去结晶水.根据图中数据,计算CuSO4xH2O中x的值为;258℃到650℃时反应的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不符合ⅦA族元素性质特征的是
A. 易形成-1价离子 B. 从上到下原子半径逐渐减小
C. 从上到下非金属性逐渐减弱 D. 从上到下氢化物的稳定性依次减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验装置的说法中正确的是( )
A.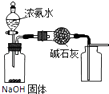
用如图装置制取干燥纯净的NH3
B.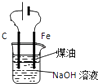
用如图装置制备Fe(OH)2并能较长时间观察其颜色
C.
用如图装置可以完成“喷泉”实验
D.
用如图装置测量Cu与浓硝酸反应产生气体的体积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业制玻璃主要原料有石英、纯碱和石灰石.在玻璃窑中发生主要反应的化学方程式为: ①Na2CO3+SiO2 ![]() Na2SiO3+CO2↑;
Na2SiO3+CO2↑;
②CaCO3+SiO2 ![]() CaSiO3+CO2↑
CaSiO3+CO2↑
(1)反应①中,被破坏的微粒间的作用力有(选填编号). a.范德华力 b.离子键 c.共价键
(2)上述两个反应的反应物和生成物中,涉及到的不同类型的晶体有种(填数字),其中熔沸点最低的化合物的电子式为;该化合物熔沸点低于CS2的原因是 .
(3)纯碱中的金属阳离子的半径比铝离子半径(填“大”或“小”);石灰石中的金属阳离子的电子所占据的电子层中,能量最高的是层(填“电子层符号”).
(4)已知10g碳酸钙完全分解,共吸收17.56KJ的热量,写出该反应的热化学方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关阿佛加德罗常数(NA)的说法错误的是
A.32 g O2所含的原子数目为NA
B.0.5 mol H2O含有的原子数目为1.5NA
C.1 mol H2O含有的H2O分子数目为NA
D.05NA个氯气分子的物质的量是0.5 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,将仪器A中的浓盐酸滴加到盛有MnO2的烧瓶中,加热后产生的气体依次通过装置B和C,然后再通过加热的石英玻璃管D(放置有铁粉).请回答: 
(1)仪器A的名称是 , 烧瓶中反应的化学方程式是 .
(2)装置B中盛放的液体是 , 气体通过装置B的目的是 . 装置C中盛放的液体是 , 气体通过装置C的目的是 .
(3)D中反应的化学方程式是 .
(4)烧杯E中盛放的液体是 , 反应的离子方程式是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com