
气体的自动化检测中常常应用原电池原理的传感器。下图为电池的工作示意图:气体扩散进入传感器,在敏感电极上发生反应,传感器就会接收到电信号。下表列出了待测气体及敏感电极上部分反应产物。则下列说法中正确的是

A.上述气体检测时,敏感电极均作电池正极
B.检测Cl2气体时,敏感电极的电极反应为: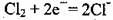
C.检测H2S气体时,对屯极充入空气,对电极上的电极反应式为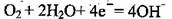
D.检测H2S和体积分数相同的两份空气样本时,传感器上产生的电流大小相同
科目:高中化学 来源: 题型:
判断正误,正确的划“√”,错误的划“×”
(1)向FeBr2溶液中通入足量氯气:2Fe2++4Br-+3Cl2===2Fe3++2Br2+6Cl- ( )
(2013·海南,10C)
(2)将水蒸气通过灼热的铁粉,铁与水在高温下反应,粉末变红 ( )
(2013·广东理综,23D)
(3)向某溶液中滴加KSCN溶液,溶液不变色,滴加氯水后溶液显红色,该溶液中一定含有Fe2+ ( )
(2013·江苏,13D)
(4)Fe3+有氧化性,所以FeCl3溶液可用于回收废旧电路板中的铜 ( )
(2012·广东理综,12D)
(5)在“硫酸亚铁铵的制备”实验中,为了得到硫酸亚铁铵晶体,应小火加热蒸发皿,直到有大量晶体析出时停止加热 ( )
(2012·浙江理综,8C)
(6)过量的Fe粉中加入稀HNO3,充分反应后,滴入KSCN溶液,溶液呈血红色,说明稀HNO3将Fe氧化为Fe3+ ( )
(2011·安徽理综,10A)
(7)Fe在足量Cl2中燃烧生成FeCl2和FeCl3 ( )
(2012·天津理综,2D)
(8)Fe分别与氯气和稀盐酸反应所得氯化物相同 ( )
(2011·重庆理综,7A)
(9)Fe与S混合加热生成FeS2 ( )
(2012·重庆理综,7A)
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)已知:
O2 (g) = O+2(g) + e-  H1= + 1175.7 kJ·mol-1
H1= + 1175.7 kJ·mol-1
PtF6(g) + e- = PtF6-(g)  H2= - 771.1 kJ·mol-1
H2= - 771.1 kJ·mol-1
O2+ PtF6-(s) = O2+(g) + PtF6-  H3= + 482.2 kJ·mol-1
H3= + 482.2 kJ·mol-1
则反应O2(g)+ PtF6 (g) = O2+PtF6- (s)  H=_____________ kJ·mol-1
H=_____________ kJ·mol-1
(2)由C和S形成的液态化合物CS2,0.2mol CS2在O2中完全燃烧,生成两种气态氧化物,298K时放出热量215kJ。 该反应的热化学方程式为________。
(3)已知:常温下0.1mol/L的某酸H2A的pH=4,则该酸为 酸(填“强”或“弱”),H2A的电离方程式为 ,该溶液中由水电离出的c(H+)= 。
(4)一定温度下,两种酸:a、盐酸 b、醋酸:
①当两种酸的物质的量浓度相同时,c(H+):a b(填“>”、“<”或“=”,下同)。
②在pH相同、体积相同的两种酸溶液中加入过量的铁粉,反应结束时生成H2的总体积:a b。
③将pH相同,体积相同的两种酸溶液分别加水稀释100倍,所得溶液的pH值:
a b
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
选项 | 实验 | 解释或结论 |
A | 用洁净的Pt丝蘸取某溶液进行焰色反应,火焰呈黄色 | 该溶液中一定含有Na+, 无K+ |
B | 用洁净的玻璃管向包有Na2O2的脱脂棉吹气,脱脂棉燃烧 | CO2、H2O与Na2O2反应是放热反应 |
C | 向溴水中滴入植物油,振荡后,油层显无色 | 溴不溶于油脂 |
D | 将硫酸酸化的H2O2滴入Fe(NO3)2溶液,溶液变黄色 | H2O2的氧化性比Fe3+强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
1909年[b20] 化学家哈伯在实验室首次合成了氨。2007年化学家格哈德·埃特尔在哈伯研究所证实了氢气与氮气在固体表面合成氨的反应过程,示意如下图:
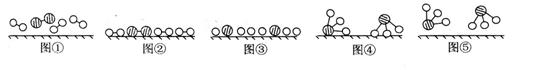
(1)图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是____▲__,__▲ ____。
(2)已知:4NH3(g) + 3O2(g) = 2N??2(g) + 6H2O(g); ΔH= - 1266.8 kJ/mol
N2(g) + O2(g) = 2NO(g) ; ΔH = + 180.5kJ/mol, 氨催化氧化的热化学方程式为___▲ _______。
(3)500℃下,在A、B两个容器中均发生合成氨的反应。隔板Ⅰ固定不动,活塞Ⅱ可自由移动。
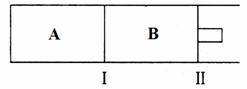
①当合成氨在容器B中达平衡时,测得其中含有1.0molN2,0.4molH2,0.4molNH3,此时容积为2.0L。则此条件下的平衡常数为_____▲ _______;保持温度和压强不变,向此容器中通入0.36molN2,平衡将____▲ ______(填“正向”、“逆向”或“不”)移动。
②向A、B两容器中均通入xmolN2和ymolH2,初始A、B容积相同,并保持温度不变。若要平衡时保持N2在A、B两容器中的体积分数相同,则x与y之间必须满足的关系式为__▲ __。
查看答案和解析>>
科目:高中化学 来源: 题型:
氧化锌是橡胶、油漆、搪瓷、电缆、医药、电子、化学等工业的重要原料。以氧
化锌粗品为原料制备活性氧化锌的生产工艺流程如下:

(1)。浸出”后得到的酸性溶液中含有Zn2+、SO42-,另含有Fe2+、Cu2+、 +、Mn2+等
+、Mn2+等
杂质。物质A的作用是调节溶液的pH至5 4,物质A最好选择________。
A.NH3.H2O B.Na2CO3 C. H2SO4 D.ZnO
已知25℃时部分金属离子从开始形成氢氧化物沉淀到沉淀完全时溶液的pH如下表:
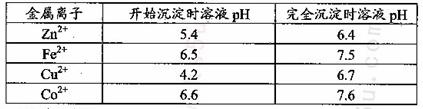
该温度下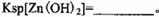 。
。
(2) KMnO4的作用是除去Mn2+和Fe2+,则KMnO4与Mn2+反应的离子方程式为_____________________________________;若溶液中 ,则处理1
,则处理1 该溶液,Fe2+所消耗的KMnO4的质量为________g(保留两位有效数字)。
该溶液,Fe2+所消耗的KMnO4的质量为________g(保留两位有效数字)。
(3)杂质Cu2+、 2+可利用置换反应除去,则物质B是_________。
2+可利用置换反应除去,则物质B是_________。
(4)被灼烧的沉淀是 ,生成该沉淀的化学方程式为________。
,生成该沉淀的化学方程式为________。
如何检验该沉淀是否洗净?________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是 ( )
A.Li是最活泼金属,F是最活泼非金属
B.Mg(OH)2碱性比Ca(OH)2强
C.元素周期表有7个主族,7个副族,1个0族,1个Ⅷ族,共16纵行
D.X2+的核外电子数目为10,则X在第3周期第ⅡA族
查看答案和解析>>
科目:高中化学 来源: 题型:
下列五种烃:①异戊烷 ②新戊烷 ③丙烷 ④正戊烷 ⑤异丁烷,其沸点按由高到低的顺序排列正确的是( )
A.①②③④⑤ B.②③④⑤①
C.⑤ ② ① ③ ④ D.④ ① ② ⑤ ③
查看答案和解析>>
科目:高中化学 来源: 题型:
金属冶炼与处理常涉及氧化还原反应。
(1)由下列物质冶炼相应金属时采用电解法的是________。
a.Fe2O3 b.NaCl c.Cu2S d.Al2O3
(2)辉铜矿(Cu2S)可发生反应:2Cu2S+2H2SO4+5O2===4CuSO4+2H2O,该反应的还原剂是________。当1 mol O2发生反应时,还原剂所失电子的物质的量为________ mol。向CuSO4溶液中加入镁条时有气体生成,该气体是______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com