
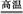 8SO2+2Fe2O3,该反应中被氧化的元素是 (填元素符号)。当该反应转移2.75 mol电子时,生成的二氧化硫在标准状况下的体积为 L。
8SO2+2Fe2O3,该反应中被氧化的元素是 (填元素符号)。当该反应转移2.75 mol电子时,生成的二氧化硫在标准状况下的体积为 L。 
 K2MnO4+MnO2+O2↑或2KClO3
K2MnO4+MnO2+O2↑或2KClO3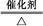 2KCl+3O2↑
2KCl+3O2↑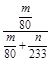 ×100%
×100% 4H++2Cl-+S
4H++2Cl-+S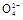
 )+c(HS
)+c(HS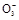 )
) 8SO2+2Fe2O3,该反应中被氧化的元素是S、Fe;设生成二氧化硫的体积是x L。
8SO2+2Fe2O3,该反应中被氧化的元素是S、Fe;设生成二氧化硫的体积是x L。 8SO2 +2Fe2O3 转移电子
8SO2 +2Fe2O3 转移电子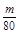 mol,装置E由于吸收了SO2而生成BaSO4白色沉淀,n(SO2)=n(BaSO4)=
mol,装置E由于吸收了SO2而生成BaSO4白色沉淀,n(SO2)=n(BaSO4)=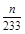 mol,由2SO2+O2
mol,由2SO2+O2 2SO3知,该反应消耗掉的n(SO2)=n(SO3)=
2SO3知,该反应消耗掉的n(SO2)=n(SO3)= 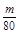 mol,所以二氧化硫的转化率为:
mol,所以二氧化硫的转化率为: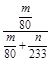 ×100%。
×100%。 )+c(HS
)+c(HS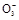 ),又溶液显中性,c(H+)=c(OH-),所以c(Na+)=2c(S
),又溶液显中性,c(H+)=c(OH-),所以c(Na+)=2c(S )+c(HS
)+c(HS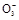 )。
)。

 黄冈创优卷系列答案
黄冈创优卷系列答案科目:高中化学 来源:不详 题型:填空题
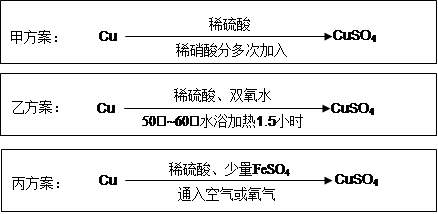
| A.CaO | B.NaOH | C.CuCO3 | D.Cu2(OH)2CO3 E.Fe2(SO4)3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 CO2(g) ?H=-283.0 kJ/mol
CO2(g) ?H=-283.0 kJ/mol SO2(g) ?H=-296.0 kJ/mol
SO2(g) ?H=-296.0 kJ/mol| A.两个反应均为氧化还原反应 |
| B.CO2与SO2可以用澄清石灰水鉴别 |
| C.CO2分子中各原子最外层均为8电子稳定结构 |
D.相同条件下:2CO(g)+SO2(g)  S(g)+2CO2 (g)?H=-270kJ/mol S(g)+2CO2 (g)?H=-270kJ/mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.SO2使溴水褪色,显示了SO2的漂白性 |
| B.SO2使溴水褪色,显示了SO2的还原性 |
| C.从溴水中提取单质溴,可以用乙醇进行萃取 |
| D.SO2是形成酸雨的唯一污染物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
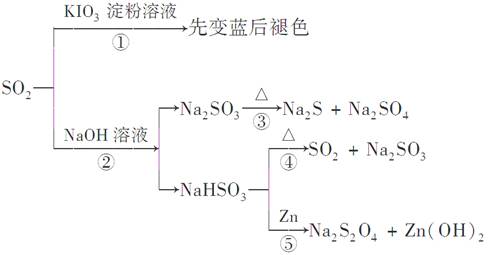
| A.反应①说明SO2具有漂白性,反应②说明SO2具有酸性 |
| B.反应②中生成物n(Na2SO3):n(NaHSO3)=1:1时,则反应物n(SO2):n(NaOH)=1:2 |
| C.反应③④⑤均属于氧化还原反应 |
| D.工业上可利用反应②和反应④回收SO2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.铜与稀硫酸,铜与浓硫酸 |
| B.铁与稀硫酸,铁与浓硫酸 |
| C.硫化钠与稀硫酸,亚硫酸钠与稀硫酸 |
| D.硫化钠与稀硫酸,硫化钠与稀盐酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
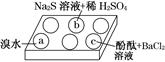
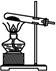
| 编号 | 实验现象 |
| a | 溴水褪色 |
| b | 产生淡黄色沉淀 |
| c | 滴入酚酞溶液变红,再加入BaCl2溶液后产生沉淀且红色褪去 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
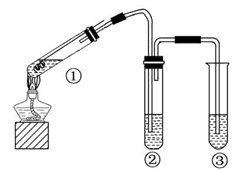
| A.上下移动①中铜丝可控制SO2的量 |
| B.②中选用品红溶液验证SO2的生成 |
| C.③中选用NaOH溶液吸收多余的SO2 |
| D.为确认CuSO4生成,向①中加水,观察颜色 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
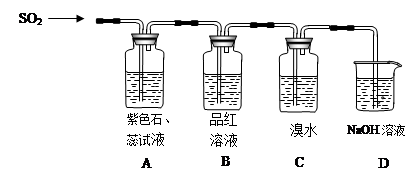
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com