


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源:2011-2012学年浙江临海市白云高级中学高一下学期期中考试化学卷(带解析) 题型:实验题
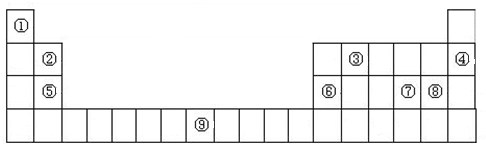
(每空1分,共6分)下面是某科学兴趣小组的同学做同周期元素性质递变规律实验时,设计的一套实验方案。其中实验步骤如下:
请整理并完成实验报告:
(1)实验目的: 。
(2)实验用品:
试剂:金属钠、镁条、铝条、稀盐酸、新制氯水、新制Na2S溶液、AlCl3溶液、NaOH溶液等。
仪器: 、酒精灯、表面皿、试管夹、镊子、小刀、玻璃片、砂纸等。
(3)实验内容(完成下列表格中的未完成的实验现象和化学方程式):
| 实验序号 | 实验现象 | 化学方程式 |
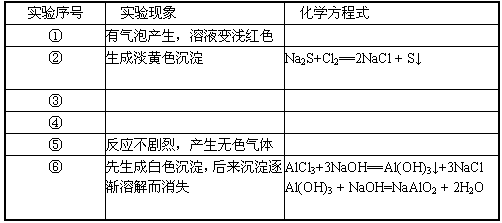
| ① | 有气体产生,溶液变成浅红色 | |
| ② | 生成浅黄色沉淀 | Na2S+Cl2=2NaCl+S↓ |
| ③ | | 2Na+2H2O=2NaOH+H2↑ |
| ④ | 剧烈反应,迅速产生无色气体 | Mg+2HCl=MgCl2+H2↑ |
| ⑤ | 反应不十分剧烈,产生无色气体 | 2Al+6HCl=2AlCl3+3H2↑ |
| ⑥ | 开始时生成白色胶状沉淀,继而沉淀消失 | AlCl3+3NaOH=Al(OH)3↓+3NaCl Al(OH)3+NaOH=NaAlO2+2H2O |
查看答案和解析>>
科目:高中化学 来源:2014届浙江临海市高一下学期期中考试化学卷(解析版) 题型:实验题
(每空1分,共6分)下面是某科学兴趣小组的同学做同周期元素性质递变规律实验时,设计的一套实验方案。其中实验步骤如下:
请整理并完成实验报告:
(1)实验目的: 。
(2)实验用品:
试剂:金属钠、镁条、铝条、稀盐酸、新制氯水、新制Na2S溶液、AlCl3溶液、NaOH溶液等。
仪器: 、酒精灯、表面皿、试管夹、镊子、小刀、玻璃片、砂纸等。
(3)实验内容(完成下列表格中的未完成的实验现象和化学方程式):
|
实验序号 |
实验现象 |
化学方程式 |
|
① |
有气体产生,溶液变成浅红色 |
|
|
② |
生成浅黄色沉淀 |
Na2S+Cl2=2NaCl+S↓ |
|
③ |
|
2Na+2H2O=2NaOH+H2↑ |
|
④ |
剧烈反应,迅速产生无色气体 |
Mg+2HCl=MgCl2+H2↑ |
|
⑤ |
反应不十分剧烈,产生无色气体 |
2Al+6HCl=2AlCl3+3H2↑ |
|
⑥ |
开始时生成白色胶状沉淀,继而沉淀消失 |
AlCl3+3NaOH=Al(OH)3↓+3NaCl Al(OH)3+NaOH=NaAlO2+2H2O |
(4)实验结论: 。
(5)请用原子结构的知识简单解释上述结论: 。
查看答案和解析>>
科目:高中化学 来源:2010年西藏拉萨中学高一第二学期期末考试化学试题 题型:填空题
(10分)今有下列两组单质,试将每组单质从不同角度进行“分类”,每种“分类”都可分别挑出一种单质,它跟其他三种单质属于不同的“类”,将挑出的单质(写化学符号)和挑选依据(写编码)列在下面相应的表格内:
两组单质为:Ⅰ.O2、F2、S、N2 Ⅱ.Fe、Na、Al、Si
“挑选依据”仅限于下述六种。该被挑出的单质跟其他三种单质不同,是由于:(A)其组成元素不属于金属(或非金属);(B)其组成元素不属于周期表中的同一族;(C)其组成元素不属于周期表中的同一周期;(D)其组成元素不属于主族(或副族)元素;(E)在常温常压下呈不同物态;(F)在常温下遇水能(或不能)迅速产生气体。
|
|
答案1 |
答案2 |
答案3 |
答案4 |
答案5 |
答案6 |
|
单质 |
Si |
|
|
|
|
|
|
挑选依据 |
A |
|
|
|
|
|
查看答案和解析>>
科目:高中化学 来源:同步题 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:
实验序号 | 实验步骤 |
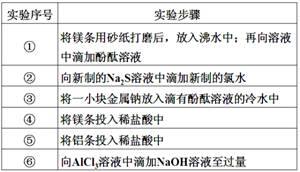
① | 将镁条用砂纸打磨后,放入沸水中;再向溶液中滴加酚酞溶液 |
② | 向新制得的Na2S溶液中滴加新制的氯水 |
③ | 将一小块金属钠放入滴有酚酞溶液的冷水中 |
④ | 将镁条投入稀盐酸中 |
⑤ | 将铝条投入稀盐酸中 |
⑥ | 向AlCl3溶液中滴加NaOH溶液至过量 |
请整理并完成实验报告。
(1)实验目的:_______________________________________________________。
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液,AlCl3溶液,NaOH溶液等。
仪器:①______________,②______________,③______________,试管夹,镊子,小刀,玻璃片,砂纸等。
(3)实验内容:(完成下列表格中的实验现象和化学方程式)
实验序号 | 实验步骤(略) | 实验现象 | 化学方程式 |
① |
|
|
|
② |
|
|
|
③ |
|
|
|
④ |
|
|
|
⑤ |
|
|
|
⑥ |
|
|
|
(4)实验结论:___________________________________________________________________。
(5)请用原子结构的知识简单解释上述结论。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com