
240 mL浓度为 0.05 mol·L-1 的Na2SO3溶液 恰好与 200mL浓度为 0.02 mol·L-1的K2X2O7溶液完全反应。已知Na2SO3可被K2X2O7氧化为Na2SO4,则元素X在还原产物中的化合价为
A、+2 B、+4 C、+5 D、+3
科目:高中化学 来源:2016届四川省高三上学期第一次月考化学试卷(解析版) 题型:填空题
(12分) HNO2是一种弱酸,且不稳定,易分解生成NO和NO2;它能被常见的强氧化剂氧化;在酸性溶液中它也是一种氧化剂,如能把Fe2+氧化成Fe3+。AgNO2是一种难溶于水、易溶于酸的化合物。试回答下列问题:
(1)人体正常的血红蛋白含有Fe2+。若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述
不正确的是________(填序号)。
A.亚硝酸盐被还原
B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+
D.亚硝酸盐是还原剂
(2)下列方法中,不能用来区分NaNO2和NaCl的是________(填序号)。
A.测定这两种溶液的pH
B.分别在两种溶液中滴加甲基橙
C.在酸性条件下加入KI—淀粉溶液来区别
D.用AgNO3和HNO3两种试剂来区别
(3)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式:_________________________。
(4) Fe与过量稀硫酸反应可以制取FeSO4。若用反应所得的酸性溶液,将Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是________(填序号)。
a.Cl2 b.Fe c.H2O2 d.HNO3
(5)若FeSO4和O2的化学计量数比为2∶1,试配平下列方程式:
FeSO4+K2O2——K2FeO4+K2O+K2SO4+O2↑
(6)高铁酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,在水中发生反应生成氢氧化铁胶体。高铁酸钾作为水处理剂发挥的作用是_____________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省高二上第一次月考化学试卷(解析版) 题型:选择题
你认为不正确的是
A.化学反应速率理念可指导怎样在一定时间内快出产品
B.化学平衡理念可指导怎样使用有限原料多出产品
C.化学反应速率理论可指导怎样提高原料的转化率
D.用速率理论和平衡理论都可提高化工生产的综合经济效益
查看答案和解析>>
科目:高中化学 来源:2016届甘肃省高三上学期第一次月考化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数,下列叙述中正确的是
A.14 g乙烯和丙烯的混合物中总原子数为3NA
B.常温下11.2 L甲烷气体含有甲烷分子数为0.5NA
C.5.6 g铁与足量的稀硫酸反应失去电子数为0.3 NA
D.0.1 mol·L-1的氢氧化钠溶液中含钠离子数为0.1NA
查看答案和解析>>
科目:高中化学 来源:2016届内蒙古赤峰市宁城县高三上学期第一次统考化学试卷(解析版) 题型:选择题
在下列指定条件的溶液中,一定能大量共存的离子组是
①K2S溶液中:SO42﹣、K+、Cl﹣、Cu2+
②水电离的c(H+)水=1.0×10﹣13mol·L﹣1的溶液中:AlO2﹣、K+、SO42﹣、Br﹣
③pH=1的溶液中:K+、Fe2+、I﹣、Br﹣
④与铝反应产生大量氢气的溶液中:Na+、K+、NH4+、NO3﹣
⑤无色溶液中:Fe2+、Na+、ClO﹣、Cl﹣
⑥能使pH试纸呈红色的溶液中:Na+、NH4+、I﹣、NO3﹣
⑦滴入KSCN溶液显血红色的溶液中:K+、Na+、SO42﹣、C6H5OH
⑧室温下,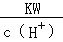 =0.1mol·L﹣1的溶液中:Na+、K+、SiO32﹣、NO3﹣.
=0.1mol·L﹣1的溶液中:Na+、K+、SiO32﹣、NO3﹣.
A.④⑦ B.②③④ C.③⑧ D.①⑤⑥
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽省高二上学期第一次月考化学试卷(解析版) 题型:选择题
某密闭容器中发生如下反应:X(g)+Y(g)  2Z(g) ΔH<0。如右图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是
2Z(g) ΔH<0。如右图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是
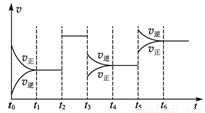
A.t2时一定加入了催化剂 B.t3时减小了压强
C.t5时一定升高了温度 D.t4~t5时间内转化率最低
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽省高一上学期第一次月考化学试卷(解析版) 题型:选择题
能正确表示下列反应的离子方程式的是
①Ba(OH)2溶液与MgSO4溶液反应:Mg2++2OH-═Mg(OH)2↓
②铁跟稀盐酸反应:Fe+2H+═Fe2++H2↑
③铁跟硫酸铜溶液反应:Fe+Cu2+═Fe2++Cu
④碳酸氢钠跟硫酸反应:2H++CO32-═CO2↑+H2O
⑤向Ba(OH)2溶液中加入NaHSO4至溶液呈中性:Ba2++2OH-+2H++SO42-═2H2O+BaSO4↓
A.②③ B.②③⑤ C.②③④⑤ D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源:2016届浙江省宁波市高三上学期10月月考化学试卷(解析版) 题型:选择题
对于实验I〜IV的描述正确的是

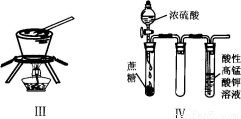
A.实验I :逐滴滴加盐酸时,试管中立即产生大量气泡.
B.实验II:充分振荡后静置,下层溶液为橙红色,上层无色
C.实验III:从饱和食盐水中提取NaCl晶体
D.装置IV:酸性KMnO4溶液中有气泡出现,且溶液颜色会逐渐变浅乃至褪去
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二上第一次月考化学试卷(解析版) 题型:填空题
汽车尾气里含有的NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致:N2(g)+O2(g) 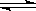 2NO(g) ΔH>0,已知该反应在2404℃时,平衡常数K=64×10-4。请回答:
2NO(g) ΔH>0,已知该反应在2404℃时,平衡常数K=64×10-4。请回答:
(1)某温度下,向2 L的密闭容器中充入N2和O2各1 mol,5分钟后O2的物质的量为0.5 mol,则NO表示的反应速率_____________。
(2)将N2、O2的混合气体充入恒温恒容密闭容器中,下列变化趋势正确的是_____________(填字母序号)。
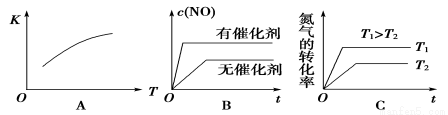
(3)向恒温恒容的密闭容器中充入等物质的量的N2和O2,达到平衡状态后再向其中充入一定量NO,重新达到化学平衡状态。与原平衡状态相比,此时平衡混合气中NO的体积分数___________。(填“变大”、“变小”或“不变”)
(4)该温度下,某时刻测得容器内N2、O2、NO的浓度分别为2.5×10-1 mol/L、4.0×10-2 mol/L和3.0×10-3 mol/L,此时反应________________(填“处于化学平衡状态”、“向正反应方向进行”或“向逆反应方向进行”),理由是____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com